Eligard 22.5 mg Enjeksiyonluk Çözelti Için S.C. Toz Içeren Şırınga ve Çözücü Içeren Şırınga Kullanma TalimatıAntineoplastik ve İmmünomodülatör Ajanlar » Hormonal Tedavi İlaçları » Hormonlar » Gonadotropin Salgılatıcı Hormon Analogları » Leuprorelin Asetat ELIGARD 22,5 mg enjeksiyonluk çözelti için s.c. toz içeren şırınga ve çözücü içeren şırınga Deri altına uygulanır.Etkin madde:Leuprorelin asetat. Enjeksiyonluk çözelti için toz ile önceden doldurulmuş bir adet şırınga (Şırınga B), 26,9 mg leuprorelin (asetat olarak) içerir. Çözücü ile sulandırıldıktan sonra verilebilen miktar 22.5 mg leuprorelin asetat'tır. Yardımcı madde(ler):Enjeksiyonluk çözelti için çözücü ile önceden doldurulmuş bir adet şırınga (Şırınga A), Poli (DL-laktik-ko-glikolit) ve N-Metilpirolidon içerir.Bu ilacı kullanmaya başlamadan önce bu KULLANMA TALİMATINI dikkatlice okuyunuz, çünkü sizin için önemli bilgiler içermektedir.Bu kullanma talimatını saklayınız. Daha sonra tekrar okumaya ihtiyaç duyabilirsiniz. Eğer ilave sorularınız olursa, lütfen doktorunuza veya eczacınıza danışınız. Bu ilaç kişisel olarak sizin için reçete edilmiştir, başkalarına vermeyiniz. Bu ilacın kullanımı sırasında, doktora veya hastaneye gittiğinizde doktorunuza bu ilacı kullandığınızı söyleyiniz. Bu talimatta yazılanlara aynen uyunuz. İlaç hakkında size önerilen dozun dışında yüksek veya düşük doz kullanmayınız.Bu Kullanma Talimatında:1.ELIGARDnedir ve ne için kullanılır ?2.ELIGARD'ı kullanmadan önce dikkat edilmesi gerekenler3.ELIGARDnasıl kullanılır ?4. Olası yan etkiler nelerdir ?5.ELIGARD'ın saklanmasıBaşlıkları yer almaktadır.1. ELIGARD nedir ve ne için kullanılır ?ELIGARD, 1 şırınga A ve 1 şırınga B'den oluşan ambalajlar halinde bulunur. Şırınga B toz halindeki etkin maddeyi, şırınga A'da etkin maddeyi sulandırmak için kullanılan çözücüyü içerir.ELIGARD, gonadotropin salgılatıcı hormon analogları olarak bilinen bir ilaç gurubunda yer alır. ELIGARD'ın etkin maddesi, erkek yetişkin hastalarda bazı cinsiyet hormonlarının üretimini engeller. ELIGARD, erişkin erkeklerde hormona duyarlı ilerlemiş prostat kanserini tedavi etmek için kullanılır. ELIGARD, hipofiz bezini kısa süreli olarak uyarır. Bu şekilde erbezlerindeki (testisler) cinsiyet hormonu üretiminin düzenlenmesinden sorumlu olan hormonların, üretimi engellenir. Böylece erkek cinsiyet hormonlarının düzeyleri azalır ve tüm tedavi boyunca aynı düzeyde kalır. ELIGARD ile tedavinin kesilmesi ile birlikte, hipofiz bezinde üretilen hormonlar ve cinsiyet hormonlarının düzeyleri kademeli olarak artarak normale döner. 2. ELIGARD'1kullanmadan önce dikkat edilmesi gerekenler ELIGARD'ı aşağıdaki durumlarda KULLANMAYINIZ:Eğer: Leuprorelin asetata veya içeriğinde bulunan yardımcı maddelerden herhangi birine alerjikseniz (aşırı duyarlılığınız varsa), Yapısal olarak cinsiyet hormonu salgılatıcı hormona benzeyen ilaçlara alerjikseniz (aşırı duyarlılığınız varsa), Ameliyatla kısırlaştırıldıysanız, ELIGARD erkek hastalarda kandaki erkek cinsiyet hormonu (serum testosteron) düzeylerinde ilave bir azalmaya yol açmaz. Sinir sisteminiz ile ilişkili belirtiler konusunda şikayetleriniz varsa (kaza, kırık veya kaymalara bağlı omurilik basısı, kanserin omuriliğe sıçraması). Bu durumda ELIGARD prostat kanseri için ancak bir başka tıbbi ürünle birlikte kullanılabilir. Eligard kadınlarda ve çocuklarda kullanılmamalıdır. ELIGARD'ı aşağıdaki durumlarda DİKKATLİ KULLANINIZ:Eğer: Tedavinin başlaması öncesinde bile, sinir sisteminiz ile ilişkili belirtiler (kaza, kırık veya kaymalara bağlı omurilikbasısı, kanserin omuriliğe sıçraması) veya idrar yollarınızdaki bir tıkanmaya bağlı olarak, idrar yapma sıkıntınız varsa, Böyle bir durumda, doktorunuz tedavinin ilk haftaları sırasında sizi yakından takip edecektir. Ayrıca; ELIGARD'ın etki mekanizmasına benzer etki gösteren diğer ilaçlarla bağlantılı olarak ciddi olay bildirimleri bulunmaktadır. Bu olaylar: omuriliğiniz üzerinde bası ve idrar yollarınızda daralmadır. Bu durumlar ölümcül veya ölümcül olmayan komplikasyonlarla birlikte olan felç durumlarına yol açabilirler. Böyle bir durumda lütfen derhal doktorunuzu bilgilendiriniz. Bu komplikasyonlar için hangi standart tedavinin uygulanacağına doktorunuz karar verecektir. Ekseriya tedavinin başlangıcında görülen belirtilerdeki kötüleşme (Olası yan etkiler bölümüne bakınız) tedavinin daha ileri safhalarında iyileşmez ise ve omurilik üzerinde bir basınç etkisi veya böbrek fonksiyonlarınızda bozukluk gelişirse, lütfen derhal doktorunuzu bilgilendiriniz. Doğal olarak mevcut, cinsiyet hormonlarının salgılanmasını etkileyen bir hormon olan gonadoliberin hormonunun etkisini taklit eden ELIGARD gibi bir ilaçla tedavi ediliyorsanız, Bu durumlarda şeker (glukoz) toleransında değişiklik olabileceğinden şeker hastalığınız (diabetes mellitus) varsa doktorunuz sizi düzenli olarak takip edecektir. Tedavinizin başlangıcında, hastalığınızla ilgili şikayetleriniz kötüleştiyse, Kemik ağrısı, idrar yollarında tıkanmaya bağlı idrar yapma güçlüğü, idrarda kan görülmesi veya kaza, kırık veya kaymalara bağlı omurilik basısına işaret eden belirtiler gibi, daha önce fark etmediğiniz yeni şikayetleriniz varsa Bu şikayetler genellikle tedavinin ilk haftasında erkek cinsiyet hormonu olan testesteronun kısa süreli olarak artmasından kaynaklanır. Tedaviye devam edildiğinde şikayetler genellikle ortadan kalkar. ELIGARD ile tedavinizin kesilmesini gerektirmezler. Doktorunuz kemik yoğunluğunuzun azaldığını (osteoporoz) söylediyse, Uzun süreli testosteron eksikliği, ilerlemiş yaş, sigara içimi, alkollü içeceklerin tüketimi, şişmanlık ve yetersiz egzersiz osteoporoza yol açabilen sebeplerdir. Kandaki düşük erkek cinsiyet hormonu (serum testosteron) düzeylerine hassas olmayan tümörleriniz varsa; ELIGARD'ın etkisinin çok zayıf olduğunu düşünüyorsanız, lütfen doktorunuzla konuşunuz. Bu uyarılar geçmişteki herhangi bir dönemde dahi olsa sizin için geçerliyse lütfen doktorunuza danışınız.ELIGARD'ın yiyecek ve içecek ile kullanılmasıUygulama yöntemi açısından yiyecek ve içeceklerle etkileşimi yoktur.Araç ve makine kullanımıAraç ve makine kullanma yeteneğiniz, tedavinin olası yan etkileri olan veya altta yatan hastalıktan kaynaklanan yorgunluk, baş dönmesi ve görme bozuklukları nedeniyle azalabilir. Bu nedenle araç ve makine kullanırken dikkatli olunmalıdır.Diğer ilaçlar ile birlikte kullanımıEğer reçeteli ya da reçetesiz herhangi bir ilacı şu anda kullanıyorsanız veya son zamanlarda kullandınız ise lütfen doktorunuza veya eczacınıza bunlar hakkında bilgi veriniz.3. ELIGARD nasıl kullanılır ?Uygun kullanım ve doz/uygulama sıklığı için talimatlarELIGARD'ı her zaman tam olarak doktorunuz tarafından tarif edildiği gibi kullanınız.Kullanıma hazırlanan ilaç size bu konuda uzmanlaşmış sağlık uzmanı tarafından uygulanacaktır. Tavsiye edilen ELIGARD dozu üç ayda bir kez uygulanan 22.5 mg'dır. Enjekte edilen çözelti, bir etkin madde deposu oluşturarak, üç ay boyunca devamlı etkin madde leuprorelin asetat salımı gerçekleştirir. Genel bir kural olarak, ELIGARD ile prostat kanserinin tedavisi uzun süreli bir tedavi gerektirir. Bundan dolayı, şikayetlerinizde bir iyileşme görülse veya tamamen ortadan kalksa bile tedaviye son vermeyiniz. ELIGARD tedavisine verilen cevap, klinik parametreler ve prostata özgü antijenin (PSA) kan düzeylerinin ölçülmesi yoluyla doktorunuz tarafından kontrol edilecektir. ELIGARD, genellikle doktorunuz veya uygun bir şekilde eğitilmiş personel tarafından uygulanacağı için, bu kişiler, kullanıma hazır çözeltinin hazırlanmasını sağlayacaklardır (bu kullanma talimatının sonunda yer alan sağlık çalışanlarına yönelik bölümde geçen talimatlara uygun olarak). Kullanıma hazır çözeltinin tarafınızca hazırlanacak olması durumunda, lütfen işlem konusundaki ayrıntılı talimatlar için doktorunuza başvurunuz. Uygulama yolu ve metoduELIGARD, hazırlandıktan sonra deri altındaki dokuya (subkutan) enjeksiyon yoluyla uygulanır.Bir atardamarın içine (intraarteriyel) veya bir toplardamarın içine (intravenöz) enjeksiyon uygulanmamalıdır.Deri altındaki dokuya enjeksiyon uygulanan diğer etkin maddelerde olduğu gibi, enjeksiyon yeri aralıklı olarak değiştirilmelidir. Bu konuda doktorunuzu uyarınız. Değişik yaş grupları:Çocuklarda kullanım:ELIGARD çocuklarda kullanılmaz.Yaşlılarda kullanımİleri yaştaki hastalarda kullanımıyla ilgili özel bir uyarı bulunmamaktadır.Özel kullanım durumlarıÖzel kullanımı yoktur.Eğer ELIGARD'ın etkisinin çok güçlü veya zayıf olduğuna dair bir izleniminiz var ise doktorunuz veya eczacınız ile konuşunuz.Kullanmanız gerekenden daha fazla ELIGARD kullandıysanız:Enjeksiyon genellikle bir sağlık uzmanı tarafından uygulandığı için doz aşımı beklenmez.Yine de gereğinden fazla miktarda uygulama yapıldıysa doktorunuz sizi özel olarak muayene edecek ve gerekli ek tedaviyi uygulayacaktır. ELIGARD'dan kullanmanız gerekenden fazlasını kullanmışsanız bir doktor veya eczacı ile konuşunuz.ELIGARD'ı kullanmayı unutursanız:Bir aylık ELIGARD uygulamanızın unutulmuş olduğuna inanıyorsanız lütfen doktorunuzla konuşunuz.Unutulan dozları dengelemek için çift doz almayınız.ELIGARD ile tedavi sonlandırıldığındaki oluşabilecek etkilerİlerlemiş prostat kanserinin tedavisi, genellikle ELIGARD ile uzun süreli bir tedavi gerektirdiği için, tedavi vaktinden önce sonlandırıldığı takdirde, hastalık ile ilişkili şikayetlerde kötüleşme görülebilir. Bu nedenle, doktorunuz tedavinizin bittiğini söylemeden ELIGARD tedavisini sonlandırmayınız.4. Olası yan etkiler nelerdir ?Tüm ilaçlar gibi ELIGARD'ın içeriğinde bulunan maddelere duyarlı olan kişilerde yan etkiler olabilir.ELIGARD ile tedavi sırasında gözlemlenen belli hormon konsantrasyonlarında artma ve azalma gibi yan etkiler, temel olarak etkin madde leuprorelin asetatın spesifik etkisine atfedilebilir. En sık tarif edilen yan etkiler enjeksiyon bölgesindeki geçici bölgesel tahrişlerin yanı sıra sıcak basmaları, kırıklık ve yorgunluktur. Hastaların yaklaşık %55'inde hafif şiddette sıcak basmaları görülmektedir. ELIGARD'ın enjeksiyonundan sonra tanımlanmış olan bölgesel yan etkiler, ekseriya tipik olarak deri altı (subkutan) yolla enjekte edilen benzer ürünler ile ilişkili olan yan etkilerle uyumludur. Enjeksiyondan hemen sonra hafif bir yanma/batma hissi çok yaygındır. Enjeksiyondan sonra ağrı, deride kızarma ve kaşınma yaygındır. Doku sertleşmesi ve ülserleşme (yara oluşması) nadirdir. Çürük, enjeksiyondan sonra yaygın olarak gözlenir. Deri altı (subkutan) enjeksiyonu takiben görülen söz konusu bölgesel yan etkiler hafiftir ve bunların kısa süreli oldukları tanımlanmıştır. ELIGARD ile tedavinin başlangıcında hastalığa özgü şikayetlerde artış görülebilir. Bu nedenle, tedaviye başladıktan sonra görülebilecek bu olası etkileri zayıflatmak amacı ile doktorunuz size tedavinin başlangıç safhasında uygun bir antiandrojen (erkek cinsiyet hormonlarının etkisini engelleyen madde) verebilir. Eğer omuriliğe sıçrama, idrar yollarında tıkanma veya idrarda kan görülmesi gibi belirtiler kötüleşirse idrar yolları ile ilgili belirtilerin kötüleşmesinin yanı sıra bacaklarda halsizlik ve/veya rahatsızlık gibi nörolojik bozukluklar görülebilir (Aynı zamanda ''ELIGARD'ı aşağıdaki durumlarda dikkatle kullanınız'bölümüne bakın.)ELIGARD ile yapılan klinik araştırmalarda karşılaşılan yan etkilerin tamamı aşağıdadır. Yan etkilerin değerlendirilmesi, aşağıdaki sıklık verilerine dayanmaktadır: -Çok yaygın: Tedavi edilen 10 kişide 1'den daha fazla -Yaygın: Tedavi edilen 100 kişide 1'den daha fazla -Yaygın olmayan: Tedavi edilen 1000 kişide 1'den daha fazla -Seyrek: Tedavi edilen 10000 kişide 1'den daha fazla -Çok seyrek: İzole vakalar dahil olmak üzere tedavi edilen 10000 kişide 1 veya daha az Bakteri, virüs ve parazitlerin neden olduğu iltihabi durumlar Yaygın olmayanİdrar yolu enfeksiyonuSeyrekLokal deri enfeksiyonuKan ve lenf sistemi hastalıkları YaygınKan tablosundaki değişiklikler (hematolojik değişiklikler)Metabolizma ve beslenme hastalıkları Yaygın olmayanŞiddetlenmiş şeker hastalığı (diabetes mellitus)Psikiyatrik hastalıklar Yaygın olmayanAnormal rüyalar, depresyon, cinsel isteksizlik (azalmış libido)Sinir sistemi hastalıkları YaygınDokunma ve acıya karşı ciltteki kısmi hassasiyet azalması (hipoestezi)Yaygın olmayanBaş dönmesi, baş ağrısı, uykusuzluk (insomnia), tat alma bozukluğu, koku alma bozukluğuSeyrekAnormal istemsiz hareketlerDamar hastalıkları Çok yaygınSıcak basmasıYaygın olmayanYüksek tansiyon (hipertansiyon), düşük tansiyon (hipotansiyon)SeyrekAni şuur kaybı ve bayılmaSolunum, göğüs bozuklukları ve mediastinal hastalıkları Yaygın olmayanBurun akıntısı (rinore)Gastrointestinal hastalıkları YaygınBulantı, karında devamlı ağrı ve hazımsızlık (dispepsi), ishal (diyare)Yaygın olmayanKabızlık (konstipasyon), ağız kuruluğuSeyrekMide gazı (flatulans), geğirme, gaz sancısıDeri ve deri altı doku hastalıkları Çok yaygınDerinin ve mukoz membranların ani kanaması, deride kızarıklıkYaygınDeri kaşıntısı (pruritus)Yaygın olmayanCiltte ıslaklık, gece terlemeleri, terleme artışıSeyrekSaç ve kıl dökülmesi (alopesi), deri döküntüsü (erupsiyonu)Kas-iskelet bozuklukları, bağ doku ve kemik hastalıkları YaygınEklemlerde ağrı (artralji)Yaygın olmayanSırt ağrısı, kas kramplarıBöbrek ve idrar hastalıkları YaygınSeyrek idrara çıkma, idrar yapmada güçlük, ağrılı idrar yapma (dizüri), gece işeme (noktüri), az idrara çıkma (oligüri)Yaygın olmayanMesane spazmı, idrarda kan görülmesi (hematüri), idrara çıkma sıklığında artış, idrar tutulması (üriner retansiyon)Genel bozukluklar ve uygulama bölgesine ilişkin hastalıkları Çok yaygınEnjeksiyon yerinde yanma, enjeksiyon yerinde karıncalanma (parestezi)YaygınBitkinlik, enjeksiyon yerinde ağrı, enjeksiyon yerinde morarma, sertlik (rigor), zayıflıkYaygın olmayanEnjeksiyon yerinde kaşıntı, uyuşukluk (letarji), ağrı, ateşÜreme sistemi ve meme hastalıkları YaygınMeme hassasiyeti, testislerde küçülme (testiküler atrofi), testis ağrısı, kısırlık (infertilite), memede büyüme (meme hipertrofisi)Yaygın olmayanErkekte meme büyümesi (jinekomasti), iktidarsızlık (impotans), testiküler bozuklukSeyrekGöğüs ağrısıAraştırmalarYaygınKandaki kreatinin fosfokinaz enziminin artması (kan kreatinin fosfokinaz artışı), kanın pıhtılaşma zamanının uzaması (uzamış koagülasyon zamanı)Yaygın olmayanKaraciğerdeki alanin aminotransferaz enziminde artış (alanin aminotransferazda artış), kan trigliseridlerinde artış, kanın pıhtılaşma faktörü olan protrombin zamanının uzaması (uzamış protrombin zamanı), kilo artışıELIGARD'ın etkin maddesiyle yapılan tedaviyle bağlantılı olarak tanımlanan diğer advers olaylar şunlardır:Üreme sistemi ve meme hastalıklarıİktidarsızlık, cinsel dürtüde azalma (her ikisi de kandaki daha düşük testosteron düzeylerinin bir sonucudur)Genel bozukluklar ve uygulama bölgesine ilişkin hastalıklarıDokuda sıvı birikimiSolunum, göğüs bozuklukları ve mediastinal hastalıklarıAkciğerdeki bir kan damarının tıkanması (pulmoner embolizm), nefes darlığıKalp hastalıklarıÇarpıntıKas-iskelet bozuklukları, bağ doku ve kemik hastalıklarıKas güçsüzlüğüSinir sistemi hastalıklarıBaş dönmesi (periferik vertigo), titremeDeri ve deri altı doku hastalıklarıDöküntüPsikiyatrik hastalıklarHafıza bozukluğu, görmede ve deri duyarlılığında bozulmaKan ve lenf sistemi hastalıkları SeyrekDoğal olarak mevcut gonadotropin hormonuna benzeyen ilaçların verilmesinden sonra hipofiz bezinde daha önceden mevcut iyi huylu tümörlere sunulan kan desteğinin eksilmesi nadiren bildirilmiştir. Nadir vakalarda trombosit ve beyaz kan hücre sayısında azalma bildirilmiştir. Glukoz toleransında değişiklik tarif edilmiştir.Doğal olarak mevcut, cinsiyet hormonlarının salgılanmasını etkileyen bir hormon olan gonadoliberin hormonunun etkisine benzer etki gösteren ELIGARD gibi bir ilaçla tedavi edilen veya bir ya da iki testisi alınmış erkeklerde kemik yoğunluğunda azalma bildirilmiştir. Bu nedenle, uzun süreli ELIGARD tedavisi yapılıyorken kemik dokusundaki azalmanın (osteoporoz) yakından izlenmesi gerekir. Osteoporoza bağlı olarak kırık riski artmaktadır. Eğer bu kullanma talimatında bahsi geçmeyen herhangi bir yan etki ile karşılaşırsanız lütfen doktorunuzu veya eczacınızı bilgilendiriniz.5. ELIGARD'ın saklanmasıELIGARD'ı çocukların göremeyeceği, erişemeyeceği yerlerde ve ambalajında saklayınız.Buzdolabında (2°C-8°C arasındaki sıcaklıklarda) ve orijinal ambalajında saklayınız. Dondurmayınız. Donmuş ürünleri çözüp kullanmayınız. Tablayı açar açmaz ürünü derhal hazırlayınız. Ürün sulandırıldıktan (hazırlandıktan) sonra hiç bekletilmeden kullanılmalıdır. Son kullanma tarihiyle uyumlu olarak kullanınız.Ambalajdaki son kullanma tarihinden sonra ELIGARD' ı kullanmayınızKullanılmayan veya son kullanma tarihi geçen ELIGARD 22.5 mg ambalajlarının atılması konusundaki talimatlar:Kullanılmayan veya son kullanma tarihi geçen ELIGARD ambalajlarını ev atığı şeklinde atmayınız. Bu konuda eczacınızdan yardım isteyiniz. Bu yaklaşım, çevre kirliliğinin azaltılmasına yardımcı olacaktır.Ruhsat Sahibi:Astellas Pharma İlaç Ticaret ve Sanayi A.Ş.Tekstilkent Koza Plaza A Blok Kat: 16 No: 60 34235 Esenler, İstanbul Tel: (0212) 440 08 00 Faks: (0212) 438 36 71 İmalatçı:Medigene AG, 82152 Planegg-Martinsried, AlmanyaBu kullanma talimatı 12/03/2009 tarihinde onaylanmıştır. AŞAĞIDAKİ BİLGİLER BU İLACI UYGULAYACAK SAĞLIK PERSONELİ İÇİNDİR İki steril kullanıma hazır şırınga derialtı enjeksiyon yoluyla hastaya uygulanmadan hemen önce karıştırılmalıdır. Şırınga B'de bulunan leuprorelin yalnızca Şırınga A'da bulunan çözücü ile karıştırılmalı; başka tıbbi ürünlerle karıştırılmamalıdır. Karıştırma işlemi aşağıdaki şekilde gerçekleştirilir: 1. Kullanımdan önce ürünün oda sıcaklığına gelmesi beklenir. Dış ambalaj (tabla) açılır ve içindekiler temiz bir alana boşaltılır (Şırınga A ve Şırınga B'yi içeren iki tabla). 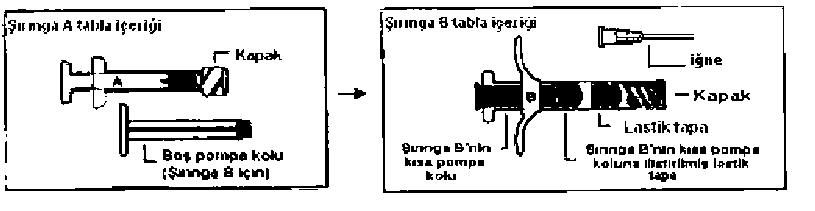 Şekil 1 Şekil 2
Şekil 1 Şekil 22. Şırınga A ve Şırınga B tablaları açıldıktan sonra, Şırınga B'den (liyofilize leuprorelin asetat) ikincil tıpa ve kısa piston çubuğu çıkarılır (Bkz. Şekil 3). Uzun piston çubuğu diğer Şırınga B tıpasına bağlanır (Bkz. Şekil 4). 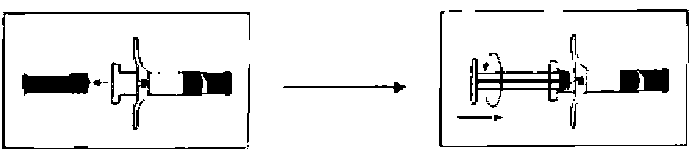 Şekil 3 Şekil 4
Şekil 3 Şekil 43. Şırınga A'nın (enjeksiyonluk çözelti için çözücü içinde sıvı polimer) başlığı ve şırınga B'nin (liyofilize leuprorelin asetat) başlıkları çıkarılır ve şırıngalar sımsıkı birleştirilir (Bkz. Şekil 5, 6 ve 7). Şırıngalar arası geçişi sağlamak ve homojen bir çözelti elde etmek için 30 kez ileri ve geri iyice sallayarak karıştırılır (Bkz. Şekil 8). Çözelti, iyice karıştırıldığında renksiz ila soluk sarı bir renk alır. 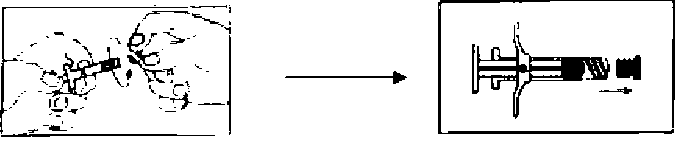 Şekil 5
Şekil 5Şekil 6 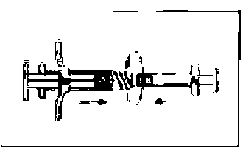 Şekil 7
Şekil 7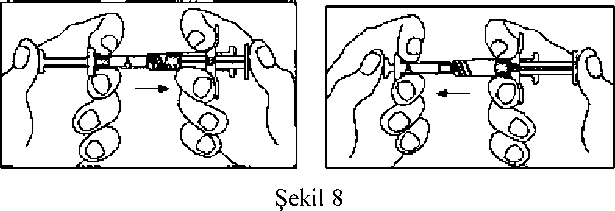 4. İçerik Şırınga B içine aktarılır. Şırınga A pistonuna kuvvetle aşağıya bastırmaya devam ederek şırıngalar birbirinden ayrılır. (Şekil 9) NOT: Formülasyon içinde küçük hava kabarcıkları kalacaktır. Bu kabul edilebilir bir durumdur ve enjeksiyonu takiben depo oluşumu üzerinde hiçbir negatif etkisi yoktur. Steril iğne, Şırınga B'ye takılır.
4. İçerik Şırınga B içine aktarılır. Şırınga A pistonuna kuvvetle aşağıya bastırmaya devam ederek şırıngalar birbirinden ayrılır. (Şekil 9) NOT: Formülasyon içinde küçük hava kabarcıkları kalacaktır. Bu kabul edilebilir bir durumdur ve enjeksiyonu takiben depo oluşumu üzerinde hiçbir negatif etkisi yoktur. Steril iğne, Şırınga B'ye takılır. Şekil 9
Şekil 95. Ürün, artık derialtı yoluyla hastaya uygulanmaya hazırdır. 6. Karıştırıldıktan hemen sonra uygulanmalıdır. 7. Yalnızca tek kullanım içindir. Kullanılmayan tüm çözelti atılmalıdır. |
İlaç BilgileriEligard 22.5 mg Enjeksiyonluk Çözelti Için S.C. Toz Içeren Şırınga ve Çözücü Içeren ŞırıngaEtken Maddesi: Leuprorelin asetat Atc Kodu: L02AE02 Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
|
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.