Idelvion 250 Iu Enjeksiyonluk Çözelti Hazırlamak İçin Toz ve Çözücü Kullanma TalimatıIDELVION 250 lU enjeksiyonluk çözelti hazırlamak için toz ve çözücü Sulandırıldıktan sonra damar içine uygulanır.Steril Etkin maddeler:Her bir flakon 250 lU albutrepenonakog alfa içerir. 2,5 mL enjeksiyonluk su ile sulandırıldıktan sonra çözelti 100 IU/mL albutrepenonakog alfa içerir. Faktör IX Çin HamsteriOvaryum hücrelerinden elde edilir.Yardımcı maddeler:Sukroz, polisorbat 80, mannitol, trisodyum sitrat dihidrat ve HCl (pH ayarlaması için)¡ Bu ilaç ek izlemeye tabidir. Bu üçgen yeni güvenlilik bilgisinin hızlı olarak belirlenmesini sağlayacaktır. Meydana gelen herhangi bir yan etkiyi raporlayarak yardımcı olabilirsiniz. Yanetkilerin nasıl raporlanacağını öğrenmek için 4. Bölümün sonuna bakabilirsiniz. Bu ilacı kullanmaya başlamadan önce bu KULLANMA TALİMATINI dikkatlice okuyunuz, çünkü sizin için önemli bilgiler içermektedir.Bu kullanma talimatım saklayınız. Daha sonra tekrar okumaya ihtiyaç duyabilirsiniz. Eğer ilave sorularımız olursa, lütfen doktorunuza veya eczacmıza danışımız. Bu ilaç kişisel olarak sizin için reçete edilmiştir, başkalarına vermeyiniz. Bu ilacın kullanımı sırasında, doktora veya hastaneye gittiğinizde doktorunuza bu ilacı kullandığınızı söyleyiniz. Bu talimatta yazılanlara aynen uyunuz. İlaç hakkında size önerilen dozun dışındayüksek veyadüşük dozkullanmayınız.Bu Kullanma Talimatında:1. IDELVION nedir ve ne için kullanılır?2. IDELVION'u kullanmadan önce dikkat edilmesi gerekenler3. IDELVION nasıl kullanılır?4. Olası yan etkiler nelerdir?5. IDELVION'un saklanmasıBaşlıkları yer almaktadır.1. IDELVION nedir ve ne için kullanılır?IDELVION, doğal kan pıhtılaşma (koagülasyon) faktörü IX'in yerine geçen bir hemofili (kanın normal olarak pıhtılaşamadığı bir hastalık) ilacıdır. IDELVION'un içerisindeki etkin maddealbutrepenonakog alfadır (albumin ile rekombinant füzyon proteinini bağlayan koagülasyon faktörüIX (rIX-FP)). Bu etkin madde rekombinant DNA teknolojisi ile üretilmektedir. Faktör IX, kan pıhtılaşması ile ilgilidir. Hemofili B hastalarında bu faktör eksiktir; bu durum kanlarının olması gerektiği kadar hızlı şekilde pıhtılaşmadığı ve dolayısıyla artan bir kanamaeğiliminin var olduğu anlamına gelir. IDELVION, hemofili B hastalarında, kanın pıhtılaşmasını sağlamak üzere faktör IX yerine geçerek etki gösterir. IDELVION, hemofili B'si (doğuştan faktör IX eksikliği veya Christmas hastalığı olarak da adlandırılır) olan tüm yaş grubundaki hastalarda, faktör IX'in eksikliğinin neden olduğu kanamayıönlemek veya durdurmak için kullanılır. IDELVION açık sarı - beyaz renkli toz olarak sunulmaktadır ve çözücü olarak enjeksiyonluk su ile birlikte tedarik edilmektedir. Enjeksiyonluk su ile birlikte sulandırılan çözelti berrak -hafif opak, sarı - renksiz olmalıdır; yani ışığa tutulduğunda parlak olabilir, fakat görünür partikül içermemelidir. Birincil ambalajTıpalı (kauçuk), diskli (plastik) ve kapaklı (alüminyum) 6 mL'lik toz içeren flakon (tip I cam) ve tıpalı (kauçuk), diskli (plastik) ve kapaklı (alüminyum) 2,5 mL'lik enjeksiyonluk su içeren flakonda(tip I cam) kullanma talimatı ile birlikte karton kutuda sunulur. Her bir kutuda; 1 adet toz içeren flakon, 1 adet 2,5 mL enjeksiyonluk çözelti, 1 adet filtre transfer cihazı 20/20 bulunur. Uygulama seti (dahili kutu): 1 adet tek kullanımlık 5 mL'lik enjektör, 1 adet kelebek infüzyon seti, 2 adet alkollü mendil, 1 adet steril olmayan plaster 2. IDELVION'u kullanmadan önce dikkat edilmesi gerekenlerIDELVION'u aşağıdaki durumlarda KULLANMAYINIZEğer; Etkin maddeye (albutropenonakog alfa) veya bu ilacın içeriğindeki diğer maddelerden (bkz.Bölüm 6) herhangi birine karşı alerjiniz varsa Hamster proteinlerine karşı alerjiniz varsa IDELVION'u aşağıdaki durumlarda DİKKATLİ KULLANINIZIDELVION'u kullanmadan önce doktorunuzla, eczacınızla veya hemşirenizle konuşunuz. Alerjik (aşırı duyarlılık) reaksiyonlar olasıdır. Ürün, eser miktarda hamster proteini içerir (ayrıcabkz. IDELVION'u aşağıdaki durumlarda kullanmayınız). Alerjik reaksiyon semptomlarımeydana gelirse, ilacı kullanmayı hemen bırakmalı ve derhal doktorunuzla görüşmelisiniz.Doktorunuz aşırı duyarlılık reaksiyonlarının erken belirtileri hakkında sizibilgilendirmelidir.Bu belirtilere; kurdeşen, genel deri döküntüsü, göğüste sıkışma, hırıltı, düşüktansiyon (hipotansiyon) ve anafilaksi (nefes almada ciddi zorluğa veya baş dönmesine neden olanciddi bir alerjik reaksiyondur) dahildir. Faktör IX ile alerjik reaksiyon riski nedeniyle; IDELVION ile başlangıç uygulamanız, alerjikreaksiyonlar için uygun tedavinin sağlanabileceği tıbbi gözlem altında gerçekleştirilmelidir. İnhibitör oluşumu(nötralize edici antikorlar), tedavi sırasında meydana gelebilen, tedavinindüzgün çalışmasını önleyen bilinen bir komplikasyondur. Eğer kanamanız IDELVION ile kontrolaltına alınamıyorsa; bu durumu derhal doktorunuza bildirin. İnhibitör gelişimi açısından dikkatlibir şekilde takip edilmeniz gerekir. Karaciğer veya kalp hastalığınız varsa ya da yakın zamanda büyük bir ameliyat geçirdiyseniz; kanpıhtılaşması komplikasyonları için risk artışı olması sebebiyle, doktorunuzu bilgilendiriniz. IDELVION enjeksiyonu için bir merkezi venöz erişim cihazına ihtiyacınız varsa; lokal enfeksiyonlar, kanda bakteri (bakteriyemi) ve kateterin yerleştirildiği kan damarında kanpıhtılaşmasıoluşumu (tromboz) gibi komplikasyon riskleri doktorunuz tarafından değerlendirilmelidir. Bu uyarılar, geçmişteki herhangi bir dönemde dahi olsa sizin için geçerliyse lütfen doktorunuza danışınız. Hamilelikhacı kullanmadan önce doktorunuza veya eczacınıza danışınız.Eğer hamileyseniz, hamile olabileceğinizi düşüyorsanız veya hamile kalmayı planlıyorsanız, bu ilacı kullanmadan önce doktor veya eczacınıza danışınız. Hamilelik döneminde IDELVION yalnızca açık bir şekilde belirtiliyor ise uygulanmalıdır. IDELVION ile tedaviniz sırasında hamile olduğunuzu fark ederseniz hemen doktorunuza veya eczacınıza danışınız.Emzirmehacı kullanmadan önce doktorunuza veya eczacınıza danışınız.Eğer emziriyorsanız, bu ilacı kullanmadan önce doktor veya eczacınıza danışınız. Emzirme döneminde IDELVION yalnızca açık bir şekilde belirtiliyor ise uygulanmalıdır. Araç ve makine kullanımıIDELVION araç ve makine kullanma yeteneğini etkilemez. Ancak baş dönmesini de içeren sersemlik haline neden olabileceğinden araç ve makine kullanımını etkileyebileceği göz önündebulundurulmalıdır. IDELVION'un içeriğinde bulunan bazı yardımcı maddeler hakkında önemli bilgilerIDELVION, maksimum dozun uygulanması durumunda (15 mL= 6000 IU) her dozunda (vücut ağırlığı 70 kg) 25,8 mg'a (1,13 mmol) kadar sodyum ihtiva eder. Bu durum, kontrollü sodyumdiyetinde olan hastalar için göz önünde bulundurulmalıdır. Kullanım kaydıBiyoteknolojik ürünlerin takip edilebilirliğinin sağlanması için uygulanan ürünün ticari ismi ve seri numarası mutlaka hasta dosyasına kaydedilmelidir. Diğer ilaçlar ile birlikte kullanımıEğer reçeteli ya da reçetesiz herhangi bir ilacı şu anda kullanıyorsanız veya son zamanlarda kullandınız ise lütfen doktorunuza veya eczacınıza bunlar hakkında bilgi veriniz.3. IDELVION nasıl kullanılır?Tedaviniz, kan pıhtılaşma rahatsızlıklarının tedavisi konusunda tecrübeli bir doktor tarafından başlatılmalı ve takip edilmelidir. Uygun kullanım ve doz/uygulama sıklığı için talimatlar:İhtiyacınız olan IDELVION dozu doktorunuz tarafından belirlenecektir. Almanız gereken IDELVION miktarı ve tedavi süresi şu koşullara bağlıdır: Hastalığınızın şiddetine Belge Takip Adresi:https://www.turkiye.gov.tr/saglik-titck-ebys Kanama bölgesine ve yoğunluğuna  Klinik durumunuza ve yanıtınıza Kilonuza Doktorunuz tarafından verilen talimatlara uyunuz. Uygulama yolu ve metodu: Genel talimatlar Toz, çözücü (sıvı) ile karıştırılmalı ve flakondan aseptik koşullar altında çekilmelidir. IDELVION, enjeksiyonluk su dışında, diğer tıbbi ürünler veya çözücüler ile karıştırılmamalıdır. Çözelti berrak ya da hafif bulanık, sarı - renksiz olmalıdır; yani ışığa tutulduğunda parlak olabilir,fakat görünür partikül içermemelidir. Filtreleme ya da enjektöre çekme işlemi sonrasında (aşağıyabakınız), çözelti kullanılmadan önce gözle kontrol edilmelidir. Çözeltinin bulanık olması veyatanecik veya partikül içermesi durumunda çözeltiyi kullanmayınız. Kullanılmamış olan tıbbi ürünler ya da atık materyaller Tıbbi Atıkların Kontrolü Yönetmeliğive Ambalaj Atıklarının Kontrolü Yönetmeliklerine uygun olarak ve doktorunuzun talimatıdoğrultusunda imha edilmelidir. SulandırmaFlakonları açmadan, IDELVION toz ve sıvısını oda veya vücut sıcaklığına getiriniz. Bu işlem, flakonların yaklaşık bir saat boyunca oda sıcaklığında bırakılması ya da flakonların birkaç dakikaboyunca avucunuzun içinde tutulması ile gerçekleştirilebilir. Flakonları doğrudan ısıya maruz BIRAKMAYINIZ. Flakonlar vücut sıcaklığının (37 °C) üzerinde ısıtılmamalıdır. Koruyucu kapaklar flakondan dikkatli şekilde çıkarılır ve açıkta kalan kauçuk tıpalar alkollü bir mendil ile temizlenir. Mix2Vial (cihaz paketi) açılmadan önce flakonlar kurumaya bırakılır ve dahasonra aşağıda verilen talimatları takip edilir. 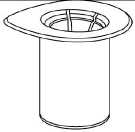
1 Mix2Vial ambalajını kapağını sıyırarak açınız. Mix2Vial'ı blister ambalajından çıkarmayınız!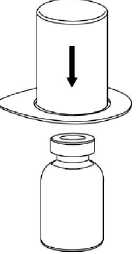 Çözücü flakonunu düz, temiz bir yüzeye yerleştiriniz ve flakonu sıkıca tutunuz. Mix2Vial'ı blister ambalajı ile birlikte kavrayıp mavi adaptör ucunu,çözücü flakon tıpası içerisinden doğrudan aşağıya doğru itiniz.
2 
4
5
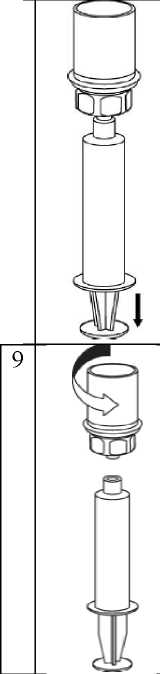
6 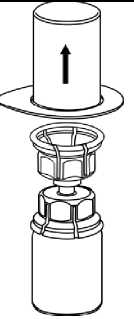 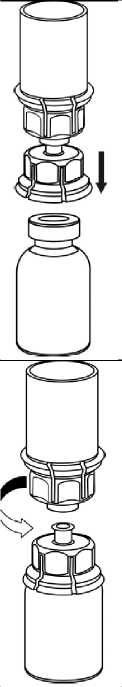 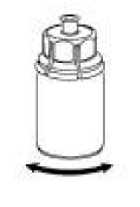 Blister ambalajı, kenarından tutarak ve dikey olarakyukarı doğru çekerek Mix2Vial'dan dikkatli şekilde çıkarınız. Mix2Vial setini değil, yalnızca blisterambalajını çektiğinizden emin olunuz.IDELVION toz flakonuşeffafdoğrudan aşağıyadoğru itiniz. Çözücü otomatik olarakIDELVION flakonu içerisine akacaktır.Bir elinizle Mix2Vial setinin IDELVION kısmını ve diğer elinizle çözücü kısmını kavrayıp seti dikkatli bir şekilde saat yönünün tersine doğru iki parçahalinde çevirerek ayırınız. İliştirilen mavi Mix2Vial adaptörü ile birlikte çözücü flakonunu çıkarınız. Madde tamamen çözünene kadar, iliştirilen şeffaf adaptör ile birlikte IDELVION flakonunu yavaşça karıştırınız. Çalkalamayınız.  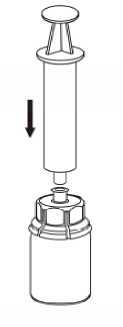 Boş steril bir enjektör içerisine hava çekiniz. IDELVION flakonu dikey konumdayken, enjektörü saat yönünde çevirerek takılan Mix2Vial'm Luerkilidine bağlayınız. Havayı IDELVION flakonuna enjekte ediniz. Enjektöre çekme ve uygulama
Enjektör pistonunu basılı tutarak, sistemi ters çevirip pistonu yavaşça geri çekerek çözeltiyi enjektöre çekiniz. Çözelti enjektöre transfer edildikten sonra, enjektör silindirini sıkıca tutunuz (enjektör pistonu aşağıda bakacak şekilde) ve saat yönünün tersine çevirerekşeffaf Mix2Vial adaptörünü enjektörden ayırınız. Ürün ile birlikte tedarik edilen damardan kan alma kiti kullanılarak, iğneyi damar içerisine yerleştiriniz. Kanın tüpün sonuna kadar akmasını bekleyiniz. Enjektörü, damardan kan alma kitinindişli kilit ucuna bağlayınız. Sulandırılmış çözeltiyiyavaşça (sizin için rahat olacak şekilde dakikada maksimum 5 mL'ye kadar)damar içerisine enjekte ediniz. Ürünün bulunduğu enjektöre kan gelmemesine dikkat ediniz.Hemen meydana gelebilecek herhangi bir yan etki bakımından kendinizi kontrol ediniz. IDELVION uygulaması ile ilişkili olabilen yan etkilerden herhangi biri ile karşılaşırsanız, enjeksiyonsonlandırılmalıdır (ayrıca bkz. Bölüm 2 ve 4). Eğer bu ilacın kullanımına ilişkin ilave sorularınız olursa, doktorunuza, eczacınıza veya hemşirenize danışınız. Belge ETogrulama Kodu: lZW56SHY3SHY3Q3NRM0FyQ3NRS3k0RG83 Belge Takip Adresi:https://www.turkiye.gov.tr/saglik-titck-ebys Değişik yaş grupları:Çocuklarda kullanımı:IDELVION tüm yaş grubundaki çocuklarda kullamlabilir. Doz, hastanın klinik durumu ve yanıtı esas alınarak ayarlanmalıdır. Yaşlılarda kullanımı:Yaşlılarda (65 yaş üzeri) pozoloji ve uygulama şekli çalışılmamıştır. Özel kullanım durumları:Böbrek yetmezliği/karaciğer yetmezliği:IDELVION'un böbrek ve/veya karaciğer yetmezliği olan hastalarda kullanımına ilişkin herhangi bir klinik çalışma yürütülmemiştir. Eğer IDELVION'un etkisinin çok güçlü veya zayıf olduğuna dair bir izleniminiz var ise doktorunuz veya eczacınız ile konuşunuz.Kullanmanız gerekenden daha fazla IDELVION kullandıysanızIDELVION'dan kullanmanız gerekenden daha fazlasını kullanmışsanız bir doktor veya eczacı ile konuşunuz.IDELVION'u kullanmayı unutursanızUnutulan dozları dengelemek için çift doz kullanmayınız.IDELVION ile tedavi sonlandırıldığında oluşabilecek etkilerIDELVION ile tedaviyi doktorunuza danışmadan sonlandırmayınız. 4. Olası yan etkiler nelerdir?Tüm ilaçlar gibi, IDELVION, içeriğinde bulunan maddelere duyarlı olan kişilerde yan etkilere neden olabilir. Aşağıdakilerden biri olursa, IDELVION'u kullanmayı durdurunuz ve DERHAL doktorunuza bildiriniz veya size en yakın hastanenin acil bölümüne başvurunuz:Eğer:Alerjik reaksiyon belirtisi fark ederseniz (aşağıdaki açıklamayı okuyunuz)ilacın etkili olmadığını fark edersenizFaktör IX ilaçları ile aşağıdaki yan etkiler gözlenmiştir: Alerjik türde aşırı duyarlılık reaksiyonlarıolasıdır (yaygın olarak) ve şu belirtileri içerebilir:kurdeşen, deri döküntüleri (genel ürtiker), göğüste sıkışma, hırıltılı solunum, düşük kan basıncı(hipotansiyon) ve anafilaksi (nefes almada ciddi zorluğa veya baş dönmesine neden olan ciddi birreaksiyondur). İnhibitörlerilaç düzgün çalışmayı durdurur (sürekli kanama) Faktör IX'e karşı bir inhibitör(nötralize edici antikor) gelişebilir, bu tür bir durumda faktör artık IX düzgün şekildeçalışmayacaktır.Bu durum gerçekleşirse ilacı bırakınız ve acilen doktorunuzla iletişime geçiniz. Bunların hepsi çok ciddi yan etkilerdir. Eğer bunlardan biri sizde mevcut ise sizin IDELVION'a karşı ^ Bubelge. ^venlı'dektroniK imza ile imzalanmıştır.ciddi alerjiniz var demektir. Acil tıbbi müdahaleye veya hastaneye yatırılmanıza gerek olabilir. Yan etkiler görülme sıklıklarına göre aşağıdaki şekilde sıralanmıştır:
Çok yaygın: Yaygın:
Yaygın olmayan: Seyrek: Çok seyrek: Bilinmiyor: 10 hastanın en az 1'inde görülebilir. 10.000 hastanın birinden az kişide görülebilir. Eldeki verilerden hareketle tahmin edilemiyor. Yaygın: Baş ağrısı Enjeksiyon bölgesi reaksiyonları Baş dönmesini de içeren sersemlik hali Alerjik reaksiyonlar (aşırı duyarlılık) Kızarıklık Yaygın olmayan: Egzama Bilinmiyor: IDELVION'a karşı nötralize edici antikorların (inhibitörler) gelişimi Çocuklarda ve ergenlerdeki yan etkiler:Çocuklardaki yan etkilerin, yetişkinlerde görülen yan etkiler ile aynı olması beklenir. Eğer bu kullanma talimatında bahsi geçmeyen herhangi bir yan etki ile karşılaşırsanız doktorunuzu veya eczacınızı bilgilendiriniz.Yan etkilerin raporlanmasıKullanma Talimatında yer alan veya almayan herhangi bir yan etki meydana gelmesi durumunda hekiminiz, eczacınız veya hemşireniz ile konuşunuz. Ayrıca karşılaştığınız yan etkileri www.titck.gov.trsitesinde yer alan "İlaç Yan Etki Bildirimi" ikonuna tıklayarak ya da 0 800 314 0008 numaralı yan etki bildirim hattını arayarak Türkiye Farmakovijilans Merkezi (TÜFAM)'nebildiriniz. Meydana gelen yan etkileri bildirerek kullanmakta olduğunuz ilacın güvenliliği hakkındadaha fazla bilgi edinilmesine katkı sağlamış olacaksınız.5. IDELVION'un saklanmasıIDELVION'u çocukların göremeyeceği, erişemeyeceği yerlerde ve ambalajında saklayınız.25 oC altındaki oda sıcaklığında ve orijinal ambalajında ışıktan koruyarak saklayınız. Ürünü dondurmayınız. Sulandırılmış ürün, hemen kullanılmalıdır .Eğer hemen kullanılmazsa kullanım içi saklama süreleri ve kullanım öncesindeki koşullar kullanıcının sorumluluğundadır.Son kullanma tarihiyle uyumlu olarak kullanınız.Belge fimmbalajov/uyaet/;ket^zgrndelblf)rtileltoIİİillanmaeiiriSindernsShOnsrawIDELVION'uagkullan-mayınız.alajov/uyaet/;ket^zgrndelblf)rtileltoIİİillanmaeiiriSindernsShOnsrawIDELVION'uagkullan-mayınız. Son kullanma tarihi geçmiş veya kullanılmayan ilaçları çöpe atmayınız! Çevre, Şehircilik ve İklim Değişikliği Bakanlığınca belirlenen toplama sistemine veriniz. Ruhsat sahibi:CSL Behring Biyoterapi İlaç Dış Ticaret A.Ş. Ü sküdar/İstanbul Üretim yeri:CSL Behring GmbH Marburg/ Almanya tarihinde onaylanmıştır.Bu kullanma talimatı |
İlaç BilgileriIdelvion 250 Iu Enjeksiyonluk Çözelti Hazırlamak İçin Toz ve ÇözücüEtken Maddesi: Albutrepenonakog Alfa Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
|
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.