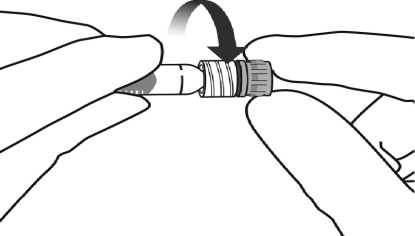
Eylea 40 Mg/ml İntravitreal Enjeksiyon İçin Çözelti İçeren Kullanıma Hazır Enjektör Kullanma TalimatıKULLANMA TALİMATIEYLEA® 40 mg/mL intravitreal enjeksiyon için çözelti içeren kullanıma hazır enjektör Göz içine (intravitreal) enjeksiyon yoluyla uygulanır.Steril Etkin madde:Her 1 mL çözelti 40 mg aflibersept içerir.Yardımcı maddeler:Polisorbat 20, sodyum fosfat monobazik monohidrat (pH ayarlaması için), sodyum fosfat dibazik heptahidrat (pH ayarlaması için), sodyum klorür, sukroz,enjeksiyonluk su.Bu ilacı kullanmaya başlamadan önce bu KULLANMA TALİMATINI dikkatlice okuyunuz, çünkü sizin için önemli bilgiler içermektedir. Bu kullanma talimatını saklayınız. Daha sonra tekrar okumaya ihtiyaç duyabilirsiniz. Eğer ilave sorularınız olursa, lütfen doktorunuza veya eczacınıza danışınız. Bu ilaç kişisel olarak sizin için reçete edilmiştir, başkalarına vermeyiniz. Bu ilacın kullanımı sırasında, doktora veya hastaneye gittiğinizde doktorunuza bu ilacıkullandığınızı söyleyiniz. Bu talimatta yazılanlara aynen uyunuz. İlaç hakkında size önerilen dozun dışındayüksekveya düşükdoz kullanmayınız._Bu Kullanma Talimatında:1. EYLEA nedir ve ne için kullanılır?2. EYLEA 'yı kullanmadan önce dikkat edilmesi gerekenler3. EYLEA nasıl kullanılır?4. Olası yan etkiler nelerdir?5. EYLEA'nın saklanmasıBaşlıkları yer almaktadır.EYLEAnedir ve ne için kullanılır? EYLEA kullanıma hazır enjektör içinde enjeksiyon için çözeltidir. Bir adet kullanımahazır enjektör içerir. Her 1 mL EYLEA çözeltisinde etkin madde olarak 40 mg aflibersept bulunur. EYLEAbir kullanıma hazır enjektörde tek doz içermektedir. Her bir tek dozluk kullanıma hazırenjektör, 2 mg aflibersept içeren 0,05 mL'lik doz uygulanmasını sağlar. EYLEA, steril, berrak, renksiz ila soluk sarı arası renkte, göz içine enjeksiyon yoluyla uygulamaya yönelik izo-ozmotik (gözünüzün içi ile eşdeğer ozmotik basınca sahip) suluçözeltidir. EYLEA'nın etkin maddesi olan aflibersept, antineovaskülarizasyon (yeni damaroluşumunu engelleyen) ilaçlar olarak adlandırılan bir ilaç grubuna aittir. Afliberseptgözün ağ tabakasında (retina; gözün ışığa duyarlı olan arka kısmı) bulunan vaskülerendotelyal büyüme faktörü-A (VEGF-A) ve plasental büyüme faktörü (PlGF) olarakbilinen bir grup proteinin aktivitesini engeller. Yaşa bağlı makula bozulması (yaş tip YBMD'si) ve uzak görme bozukluğu ile birliktegörülen yeni damar oluşumu (miyopik koroidal neovaskülarizasyonu, miyopik KNV'si)olan hastalarda aşırı miktarlarda bulunan bu faktörler gözde normal olmayan, yeni kandamarlarının oluşumuna neden olurlar. Bu yeni kan damarları, kan bileşenlerinin göze 1 / 16sızmasına ve bunun neticesinde gözde bulunan, görme işlevinden sorumlu dokularda hasara neden olabilirler. Retinal ven dal oklüzyonu (RVDO) hastalarında; retinadan kanı uzağa taşıyan ana kan damarlarının bir ya da daha fazla dalında tıkanma meydana gelir. Bu duruma cevabenVEGF düzeyleri yükselerek retinaya sıvı sızmasına ve buna bağlı maküler ödeme nedenolurlar. Santral retinal ven oklüzyonu (SRVO) olan hastalarda, kanı retinadan uzaklaştıran ana kan damarında tıkanma meydana gelir. Bu duruma cevaben VEGF düzeyleri yükselerekretinaya sıvı sızmasına ve buna bağlı olarak da makulada (sarı nokta) şişmeye nedenolurlar; buna maküler ödem (gözün arka tarafında şişme) adı verilir. Makula sıvı ileşişince, merkezi görme bulanık hale gelir. Diyabetik makula ödemi (DMÖ), makula içindeki kan damarlarından sıvı sızıntısı nedeniyle diyabet hastalarında meydana gelen retina şişmesidir. Makula, retinanın iyigörmeden sorumlu kısmıdır. Makula sıvıyla şiştiğinde, merkezi görme bulanıklaşır. EYLEA'nın gözde normal olmayan yeni kan damarlarının oluşumunu ve retinaya sızan sıvı ve kan miktarını azalttığı gösterilmiştir. EYLEA, yaş tip YBMD, SRVO, RVDO,DMÖ ve miyopik KNV ile ilişkili görüş kaybının ilerlememesine yardımcı olur vebirçok hastada görüş kaybında düzelme sağlar. EYLEA, yetişkinlerde aşağıdaki göz rahatsızlıklarının tedavisi için göz içine enjeksiyon yoluyla uygulanır: - Neovasküler (yaş tip) yaşa bağlı makula bozulması (YBMD), - Retinal damar tıkanıklığına (RVDO ya da SRVO) sekonder gelişen maküler ödem, - Diyabetik makula ödeminden (DMÖ) kaynaklanan görme bozukluğu, - Miyopik koroidal neovaskülarizasyona (miyopik KNV) bağlı görme bozukluğu. 2. EYLEA'yı kullanmadan önce dikkat edilmesi gerekenlerEYLEA'yı aşağıdaki durumlarda KULLANMAYINIZEğer; Aflibersepte veya EYLEA'nın bileşiminde bulunan yardımcı maddelerden herhangi birine karşı alerjiniz (aşırı duyarlılığınız) varsa, Gözünüzde şiddetli iltihaplanma varsa (belirtileri ağrı ve kızarıklıktır), Gözünüzün içinde ya da çevresinde bir enfeksiyon varsa (oküler veya periokülerenfeksiyon). EYLEA'yı aşağıdaki durumlarda DİKKATLİ KULLANINIZEYLEA size uygulanmadan önce doktorunuzla konuşunuz: Eğer; Glokomunuz (göz içi basıncının artması) varsa, Işık çakmaları veya uçuşan cisimler görme öykünüz varsa veya uçuşan cisim boyutu ve sayısında ani bir artış varsa, Geçen dört hafta içinde gözünüz ameliyat edildiyse veya gelecek dört hafta içinde böyle bir ameliyat planlanıyorsa, Göz damarlarınızdaki tıkanıklık ileri seviyedeyse (iskemik kronik SRVO ya da RVDO) 2 / 16EYLEA tedavisi tavsiye edilmemektedir. Ayrıca, aşağıdakileri de bilmenizde fayda vardır: Her iki göze eş zamanlı EYLEA uygulanmasının güvenliliği ve etkililiği üzerine sistematik olarak çalışılmamıştır ve bu şekilde kullanılırsa, genel yan etkilerin görülme riskinde artışaneden olabilir. EYLEA enjeksiyonu bazı hastalarda enjeksiyondan sonraki 60 dakika içinde göz içi basıncında (intraoküler basınç) artışa yol açabilir. Doktorunuz her enjeksiyondan sonra budurumun takibini yapacaktır. Gözünüzün içinde enfeksiyon veya enflamasyon (endoftalmit) veya başka komplikasyonlar gelişirse, göz ağrısı veya artan rahatsızlık hissi, göz kızarıklığında kötüleşme, bulanık veyaaz görme ve ışığa karşı hassasiyette artış yaşayabilirsiniz. Tüm belirtilerin mümkünolduğunca kısa sürede teşhis ve tedavi edilmesi önemlidir. Doktorunuz gözünüzün arkasında yer alan tabakaların birinde yırtılma veya ayrılma (retinaayrılması veya yırtılması ve retinal pigment epitel ayrılması veya yırtılması) ihtimaliniartırabilecek diğer risk faktörlerinin olup olmadığını kontrol edecektir, bu tür durumlardaEYLEA'nın dikkatli bir şekilde kullanılması gerekir. Potansiyel faydası, doğmamış çocuğa yönelik potansiyel riskine ağır basmadığı sürece EYLEA hamilelikte kullanılmamalıdır. Çocuk doğurma potansiyeli olan kadınlar tedavi sırasında ve son EYLEA enjeksiyonundansonra en az üç ay daha etkili bir doğum kontrol yöntemi kullanmalıdır. EYLEA'nın içeriğinde bulunanlara benzer içerikleri olan VEGF inhibitörlerinin sistemik kullanımında, kalp krizi veya inmeye neden olabilecek kan pıhtılarının kan damarlarınıtıkama (arteriyel tromboembolik olaylar) riski vardır. Göze yapılan EYLEA enjeksiyonundansonra bu tür olayların meydana gelmesine ilişkin teorik bir risk söz konusudur. Son 6 ayiçinde inme, mini inme (geçici iskemik atak) veya kalp krizi geçiren SRVO, RVDO, DMÖ vemiyopik KNV hastalarının tedavisinde güvenlilik ile ilgili veriler sınırlıdır. Bunlardanherhangi biri sizin için geçerliyse, EYLEA dikkatli bir şekilde uygulanacaktır. Aşağıdaki hastaların tedavisi ile ilgili deneyim sınırlıdır: Tip 1 diyabet kaynaklı DMÖ hastaları, çok yüksek ortalama kan şekeri değerleri olan (%12 üzeri HbA1c) diyabet hastaları, proliferatif diyabetik retinopati olarak adlandırılan diyabet kaynaklı bir göz hastalığı olandiyabet hastaları. Aşağıdaki hastaların tedavisi ile ilgili hiç deneyim yoktur: Aktif sistemik enfeksiyonları olan hastalar, Retinada ayrılma veya makulada delik gibi diğer göz hastalıkları olan hastalar, Kontrol edilemeyen yüksek kan basıncı olan diyabet hastaları, Asya popülasyonuna ait olmayan miyopik KNV hastaları, Miyopik KNV için daha önce tedavi görmüş hastalar, Makulanın merkez bölgesinin dışında hasarı olan miyopik KNV hastaları (ekstrafoveal lezyon). Yukarıda belirtilen durumlardan herhangi biri sizin için geçerliyse, doktorunuz sizi EYLEA ile tedavi ederken bu bilgi eksikliğini göz önünde bulunduracaktır. Biyoteknolojik ürünlerin takip edilebilirliğinin sağlanması için uygulanan ürünün ticari ismi ve seri numarası açık bir şekilde kaydedilmelidir. 3 / 16 Bu uyarılar geçmişteki herhangi bir dönemde dahi olsa sizin için geçerliyse lütfen doktorunuza danışınız. EYLEA'nın yiyecek ve içecek ile kullanılmasıEYLEA'nın yiyecek ve içecek ile kullanılmasına ilişkin herhangi bir etkileşim çalışması gerçekleştirilmemiştir. Hamilelikİlacı kullanmadan önce doktorunuza veya eczacınıza danışınız.EYLEA'nın hamile kadınlarda kullanımına ilişkin veri mevcut değildir. Bu nedenle EYLEA'nın anneye sağlayacağı muhtemel yarar, anne karnındaki bebek üzerindeki muhtemelriske ağır basmadığı sürece hamilelik döneminde kullanılmamalıdır. Eğer hamileyseniz ya dahamile kalmayı planlıyorsanız, EYLEA ile tedaviye başlamadan önce doktorunuza bilgiveriniz. Hamile kalma olasılığı olan kadınlar, tedavi süresince ve son intravitreal EYLEAenjeksiyonundan sonra en az 3 ay boyunca etkili bir doğum kontrol yöntemi kullanmalıdırlar. Tedaviniz sırasında hamile olduğunuzu fark ederseniz hemen doktorunuza veya eczacınıza danışınız.Emzirmeİlacı kullanmadan önce doktorunuza veya eczacınıza danışınız.Afliberseptin insanlarda süte geçip geçmediği bilinmemektedir. Bu nedenle EYLEA'nın emzirme döneminde kullanılması önerilmez. EYLEA tedavisine başlamadan önce doktorunuza danışınız. Emzirmenin ya da EYLEA tedavisinin kesilip kesilmeyeceği yönünde bir karar verilmelidir. Araç ve makine kullanımıEYLEA uygulamasından sonra bazı geçici görme bozuklukları yaşayabilirsiniz. Bu bozukluklar devam ettiği sürece araç veya makine kullanmayınız. EYLEA'nın içeriğinde bulunan bazı yardımcı maddeler hakkında önemli bilgilerBu tıbbi ürün her dozunda 1 mmol (23 mg)'den daha az sodyum ihtiva eder; yani esasında sodyum içermediği kabul edilebilir. Diğer ilaçlar ile birlikte kullanımıEğer reçeteli ya da reçetesiz herhangi bir ilacı şu anda kullanıyorsanız veya son zamanlarda kullandınız ise lütfen doktorunuza veya eczacınıza bunlar hakkında bilgi veriniz.EYLEA ile herhangi bir ilaç etkileşim çalışması yürütülmemiştir. 3. EYLEA nasıl kullanılır?Uygun kullanım ve doz/uygulama sıklığı için talimatlar:Önerilen doz 2 mg aflibersepttir (0,05 mL). Yaş tip YBMD Yaş tip YBMD bulunan hastalarda tedavi, ardışık üç doz olarak ayda bir kez tek enjeksiyonu takiben iki ayda bir tek enjeksiyon şeklinde uygulanması önerilir. 4 / 16Doktorunuzun görmeyle ilgili ve/veya anatomik sonuçlarla ilgili takdirine göre, tedavi aralığınız iki ay olarak korunabilir veya tedavi et ve uzat adlı bir dozlama rejimi kullanılarakuzatılabilir, bu yaklaşımda görmeyle ilgili ve/veya anatomik stabil sonuçların korunması içinenjeksiyon aralıkları 2 veya 4 haftalık kademelerle uzatılabilir. Durumunuz kötüleşirse, enjeksiyon aralıkları kısaltılabilir. Herhangi bir problem yaşamazsanız veya doktorunuz tarafından farklı şekilde tavsiye edilmedikçe, enjeksiyonlar arasında doktorunuzu görmenize gerek yoktur. RVO'ya sekonder makula ödemi (RVDO veya SRVO) Sizin için en uygun tedavi programını doktorunuz belirleyecektir. Tedaviniz bir seri aylık EYLEA enjeksiyonu ile başlayacaktır. İki enjeksiyon arasında geçen süre bir aydan kısa olmayacaktır. Tedavinin devam ettirilmesi sizin için yarar sağlamayacaksa, doktorunuz EYLEA tedavisini sonlandırmaya karar verebilir. Durumunuz stabil olana kadar tedaviniz aylık enjeksiyonlarla devam edecektir. Ayda bir kez uygulanan üç veya daha fazla enjeksiyon gerekebilir. Doktorunuz tedaviye verdiğiniz yanıtı izleyecektir ve tedavinizi sürdürürken hastalığınız stabil hale gelince bu durumunuzu devam ettirmek için enjeksiyonlar arasında geçen süreyikademeli olarak uzatabilir. Tedavi aralığının uzatılmasıyla durumunuzda kötüleşme olmasıhalinde, doktorunuz bu aralığı uygun şekilde kısaltacaktır. Tedaviye verdiğiniz yanıta göre doktorunuz takip amaçlı muayene ve tedavilerin programına ilişkin karar verecektir. Diyabetik makula ödemi (DMÖ) DMÖ bulunan hastalarda tedavi ardışık beş doz olarak ayda bir kez tek enjeksiyon ile başlatılır ve sonrasında iki ayda bir tek enjeksiyon şeklinde uygulanması önerilir. Doktorunuzun muayenesine göre, tedavi aralığı iki ayda bir tutulabilir veya durumunuza göre ayarlanabilir. Doktorunuz takip muayenelerinin takvimine karar verecektir. Devam eden tedaviden fayda görmediğiniz belirlenirse, doktorunuz EYLEA ile tedaviyi durdurmaya karar verebilir. Tedavinin devam ettirilmesinin sizin için yarar sağlamayacağı belirlendiği takdirde, doktorunuz EYLEA tedavisini sonlandırmaya karar verebilir. Miyopik KNV Miyopik KNV bulunan hastalarda tedavi tek bir enjeksiyonla uygulanacaktır. Ancak doktorunuzun yaptığı muayeneler durumunuzun düzelmediğini gösterdiği takdirde daha fazlaenjeksiyon uygulanabilir. İki enjeksiyon arasında geçen süre bir aydan kısa olmayacaktır. 5 / 16 Uygulama yolu ve metodu:EYLEA, göz içine (intravitreal) enjeksiyon yoluyla uygulanır. EYLEA, göz içine enjeksiyonların uygulanmasında deneyimli bir uzman hekim tarafından uygulanmalıdır. EYLEA, size aseptik (temiz ve steril) koşullar altında enjekte edilecektir. Enjeksiyondan önce doktorunuz, enfeksiyonu önlemek amacıyla dezenfektan bir göz yıkama solüsyonu kullanarakgözünüzü dikkatle temizleyecektir. Doktorunuz ayrıca enjeksiyon nedeniyleyaşayabileceğiniz ağrıyı azaltmak ya da önlemek üzere size lokal anestezi (bölgesel anestezi)uygulayabilir. Değişik yaş grupları:Çocuklarda kullanımı:Yaşa bağlı makula bozulması (yaş tip YBMD'si), santral retinal ven oklüzyonu (SRVO), retinal ven dal oklüzyonu (RVDO), diyabetik makula ödemi (DMÖ) ve miyopik koroidalneovaskülarizasyon (miyopik KNV) genel olarak yetişkin popülasyonda görüldüğündenEYLEA'nın çocuklarda ve 18 yaşından küçük ergenlerde etkililiği ve güvenliliğiçalışılmamıştır. Bu yaş grubunda kullanımı söz konusu değildir. Yaşlılarda kullanımı:EYLEA yaşlılarda doz ayarlaması yapılmadan kullanılabilir. 75 yaş üzerindeki DMÖ hastalarında deneyim sınırlıdır. Özel kullanım durumları:Böbrek yetmezliği:Böbrek yetmezliği olan hastalarda çalışma yapılmamıştır. Eldeki veriler dikkate alındığında, böbrek yetmezliği olan hastalar için EYLEA dozunda ayarlama yapılması gerekli değildir. Karaciğer yetmezliği:Karaciğer yetmezliği olan hastalarda çalışma yapılmamıştır. Eldeki veriler dikkate alındığında, karaciğer yetmezliği olan hastalar için EYLEA dozunda ayarlama yapılması gerekli değildir. Eğer EYLEA 'nın etkisinin çok güçlü veya zayıf olduğuna dair bir izleniminiz var ise doktorunuz veya eczacınız ile konuşunuz.Kullanmanız gerekenden daha fazla EYLEA kullandıysanız:Daha yüksek enjeksiyon hacmi ile doz aşımı, göz içi basıncını yükseltebilir. Bu nedenle, doz aşımı vakalarında göz içi basıncı takip edilmeli ve tedaviden sorumlu hekimin gerekli görmesihalinde uygun tedavi başlatılmalıdır. EYLEA 'dan kullanmanız gerekenden fazlasını kullanmışsanız bir doktor veya eczacı ile konuşunuz.6 / 16 EYLEA'yı kullanmayı unutursanız:Muayene ve enjeksiyon için yeni bir randevu alınız. Unutulan dozları dengelemek için çift doz uygulamayınız.EYLEA ile tedavi sonlandırıldığında oluşabilecek etkiler:EYLEA tedavisini bırakmayı düşünüyorsanız, önce doktorunuza danışınız. Bu ürünün kullanımıyla ilgili başka sorularınız varsa, doktorunuza sorunuz. 4. Olası yan etkiler nelerdir?Tüm ilaçlar gibi, EYLEA'nın içeriğinde bulunan maddelere duyarlı olan kişilerde yan etkiler görülebilir. Aşağıdakilerden biri olursa EYLEA'yı kullanmayı durdurunuz ve DERHAL doktorunuza bildiriniz veya size en yakın hastanenin acil bölümüne başvurunuz.Alerjik reaksiyon (kaşıntı, döküntü, göz kapağı ödemi gibi belirtileri olan aşırı duyarlılık) gelişme ihtimali bulunmaktadır. Bunların hepsi ciddi yan etkilerdir. Eğer bunlardan biri sizde mevcut ise, acil tıbbi müdahaleye veya hastaneye yatırılmanıza gerek olabilir. Aşağıdakilerden herhangi birini fark ederseniz, hemen doktorunuza bildiriniz veya size en yakın hastanenin acil bölümüne başvurunuz: EYLEA uygulaması ile birlikte, enjeksiyon işlemine bağlı gözleri etkileyen bazı yan etkiler ortaya çıkabilir. Bu yan etkilerden bazıları ciddi olabilir ve bunlar arasında körlük, gözmerceğinde bulanıklaşma (katarakt), göz içine kanama (vitreus kanaması), gözünarkasındaki ışığa duyarlı tabakanın ayrılması, yırtılması veya kanaması (retinadekolmanı veya yırtığı), göz içindeki jel benzeri maddenin retinadan ayrılması (vitreusdekolmanı), göz içinde ciddi enfeksiyon veya iltihaplanma (endoftalmit), ve göz içibasıncının yükselmesi yer almaktadır. Klinik çalışmalarda gözleri etkileyen bu ciddi yanetkiler her 1900 enjeksiyonun 1'inden seyrek gözlenmiştir. Bunların hepsi ciddi yan etkilerdir. Acil tıbbi müdahale gerekebilir. Eğer enjeksiyondan sonra görmede ani bir düşüş ya da gözde ağrıda ve kızarıklıkta bir artış yaşıyorsanız, derhaldoktorunuza başvurunuz. Yan etkiler aşağıdaki kategorilerde gösterildiği şekilde sıralanmıştır: Çok yaygın: 10 hastanın en az 1'inde görülebilir. Seyrek: 1.000 hastanın birinden az, fakat 10.000 hastanın birinde veya birinden fazla görülebilir. Çok seyrek: 10.000 hastanın birinden az görülebilir. Bilinmiyor: Eldeki veriler ile tahmin edilememektedir. 7 / 16Aşağıdakilerden herhangi birini fark ederseniz, doktorunuza söyleyiniz:Bildirilen yan etkilerin listesi:Enjeksiyon işlemi ya da ilaç ile muhtemelen ilişkili olduğu bildirilen yan etkilerin listesi aşağıda verilmektedir. Lütfen telaşlanmayınız; bunlardan hiçbirini yaşamayabilirsiniz.Şüphelendiğiniz yan etkileri her zaman doktorunuzla konuşunuz. Çok yaygın Görmede bozukluk (görüş keskinliğinde azalma) Gözün arka tarafında kanama (retinal hemoraji) Gözün dış katmanlarındaki ince kan damarlarındaki kanamanın neden olduğu gözde kan toplanması (konjunktival hemoraji) Göz ağrısı Yaygın Yüzen cisimler ve ışık çakması ile sonuçlanan ve bazen görme kaybına kadar ilerleyebilengözün arka kısmındaki tabakalardan birinin ayrılması veya yırtılması (retina pigmentepitelinin yırtılması*, retina pigment epitel dekolmanı*) Retinada bozulma (dejenerasyon) (görmenin bozulmasına yol açabilir) Göz içine kanama (vitreus kanaması) Göz merceğinde bulanıklaşmanın belirli türleri (katarakt, nükleer katarakt, subkapsüler katarakt, kortikal katarakt) Göz küresinin ön tabakasında hasar (kornea erozyonu, kornea abrazyonu) Göz içi basıncının yükselmesi (intraoküler basınç artışı) Bulanık görme Görüş alanında hareket eden noktalar (vitreusta uçuşan noktalar) Göz içindeki jel benzeri maddenin retinadan ayrılması (vitreus dekolmanı, uçuşan noktalarve ışık çakmaları ile sonuçlanan) Enjeksiyon yerinde ağrı Gözün içinde bir şey olması hissi (gözlerde yabancı cisim hissi) Gözyaşı üretiminde artış (lakrimasyon artışı) Göz kapağında şişme (göz kapağı ödemi) Enjeksiyon yerinde kanama (enjeksiyon yerinde hemoraji) Bulanık görme ve iltihaplı göz ile sonuçlanan göz küresinin ön tabakasında (kornea) iltihaplanma (punktat keratit) Gözde kızarıklık (konjunktival hiperemi, oküler hiperemi) Yaş tip YBMD ile ilişkili olduğu bilinen durumlardır; sadece yaş tip YBMD hastalarında gözlenmiştir. Yaygın olmayan Alerjik reaksiyonlar (aşırı duyarlılık)*** Göz içinde ciddi enfeksiyon veya iltihaplanma (endoftalmit)** Retinada ayrılma, retina yırtılması Gözün iris bölümünde iltihaplanma (iritis) Gözün belirli kısımlarının iltihaplanması (üveit, iridosiklit, ön kamarada bulanıklık) Göz merceğinde bulanıklaşmanın belirli türleri (lentiküler opasiteler) Göz küresinin ön tabakasında hasar (kornea epitel defekti) 8 / 16 Enjeksiyon yerinde tahriş Gözde anormal his Göz kapağı iritasyonu Göz küresinin ön tabakasında şişme (kornea ödemi) ** Kültür pozitif ve kültür negatif endoftalmit *** Kızarıklık benzeri alerjik reaksiyonlar, döküntü, kaşıntı (pirürit), kurdeşen (ürtiker) ve birkaç ciddi alerji vakası (anafilaktik / anaflaktoid) reaksiyonları bildirilmiştir. Seyrek Körlük Göze gelen travma nedeniyle lenste bulanıklaşma (travmatik katarakt) Gözdeki jel benzeri maddenin iltihaplanması (vitrit) Gözde irin (hipopiyon) Klinik çalışmalarda, yaş tip YBMD bulunan ve kan sulandırıcı kullanan hastalarda gözün dış tabakalarındaki küçük kan damarlarında kanama (konjonktival hemoraji) insidansının arttığıkaydedilmiştir. Bu insidans artışının ranibizumab (yeni damar oluşumunu engelleyen bir ilaç)ve EYLEA tedavisi alan hastalar için benzer olduğu görülmüştür. EYLEA içeriğinde bulunanlara benzer maddeler olan VEGF inhibitörlerinin tüm vücudu etkileyen şekilde genel kullanımı, olası kan pıhtılarının kan damarlarını tıkaması durumu(arteriyel tromboembolik olay) riski ile ilişkilidir. Bu olaylar kalp krizine veya inmeye nedenolabilir. EYLEA'nın göz içine enjeksiyonundan sonra bu tür olaylar yönünden teorik bir riskmevcuttur. Tüm tedavi edici proteinlerde olduğu gibi EYLEA ile de olası bağışıklık sistemi reaksiyonu (antikor üretimi) söz konusudur. EYLEA uygulanmasının ardından çok seyrek olarak görüş alanında silikon yağıyla ilişkili hareket eden noktalar (uçuşan noktalar) bildirilmiştir. Eğer bu kullanma talimatında bahsi geçmeyen herhangi bir yan etki ile karşılaşırsanız doktorunuzu veya eczacınızı bilgilendiriniz.Yan etkilerin raporlanmasıKullanma Talimatında yer alan veya almayan herhangi bir yan etki meydana gelmesi durumunda hekiminiz, eczacınız veya hemşireniz ile konuşunuz. Ayrıca karşılaştığınız yanetkileri www.titck.gov.tr sitesinde yer alan İlaç Yan Etki Bildirimi ikonuna tıklayarak yada 0 800 314 00 08 numaralı yan etki bildirim hattını arayarak Türkiye FarmakovijilansMerkezi (TÜFAM)'ne bildiriniz. Meydana gelen yan etkileri bildirerek kullanmaktaolduğunuz ilacın güvenliliği hakkında daha fazla bilgi edinilmesine katkı sağlamışolacaksınız. 5. EYLEA'nın saklanmasıEYLEA 'yı çocukların göremeyeceği, erişemeyeceği yerlerde ve ambalajında saklayınız.9 / 16Son kullanma tarihi ile uyumlu olarak kullanınız.Ambalajın üzerindeki son kullanma tarihinden sonra EYLEA 'yı kullanmayınız.Son Kull. Ta.: ibaresinden sonra yazılan rakam ayı temsil eder ve o ayın son günü son kullanım tarihidir. Eğer üründe ve/veya ambalajında bozukluklar fark ederseniz EYLEA'yıkullanmayınız. Son kullanma tarihi geçmiş veya kullanılmayan ilaçları çöpe atmayınız! Çevre, Şehircilik ve İklim Değişikliği Bakanlığınca belirlenen toplama sistemine veriniz. Ruhsat sahibi:Tel:Faks:0216 645 39 50Üretim yeri:Regeneron Pharmaceuticals, Inc. Rensselaer/New York/Amerika Birleşik DevletleriBu kullanma talimatı 27/10/2022 tarihinde onaylanmıştır.10 / 16 AŞAĞIDAKİ BİLGİLER EYLEA'YI UYGULAYACAK SAĞLIK PERSONELİ İÇİNDİREYLEA yalnızca intravitreal enjeksiyon içindir. EYLEA, intravitreal enjeksiyon uygulamasında deneyimli, göz hastalıkları uzmanı olan bir hekim tarafından uygulanmalıdır. Pozoloji/uygulama sıklığı ve süresi:Yaş tip YBMD (yaşa bağlı makula dejenerasyonu) Önerilen EYLEA dozu, 0,05 mL'ye eşdeğer 2 mg aflibersepttir. EYLEA tedavisinin, birbirini takip eden üç doz şeklinde ayda bir kez tek enjeksiyon olarak başlatılması ve daha sonra, tedavi aralığının iki ay olacak şekilde uzatılması önerilir. Hekimin görmeyle ilgili ve/veya anatomik sonuçlara ilişkin değerlendirmesi doğrultusunda, tedavi aralığı iki ay olarak kalabilir ya da tedavi et ve uzat dozlama rejimi kullanılarakuzatılabilir, bu yaklaşımda görmeyle ilgili ve/veya anatomik sonuçların korunması içinenjeksiyon aralıkları 2 veya 4 haftalık kademelerle artırılır. Görmeyle ilgili ve/veya anatomik sonuçlarda kötüleşme olması halinde, tedavi aralığı uygun şekilde kısaltılmalıdır. Enjeksiyonlar arasında izlem yapılması gerekmez. Hekimin takdirine göre, izlem vizitlerinin programı enjeksiyon vizitlerinden daha sık olabilir. Enjeksiyonlar arasında dört aydan uzun veya 4 haftadan kısa tedavi aralıkları değerlendirilmemiştir. RVO'ya sekonder makula ödemi (RVDO veya SRVO) Önerilen EYLEA dozu, 0,05 mL'ye eşdeğer 2 mg aflibersepttir. İlk enjeksiyondan sonra, tedavinin ayda bir kez uygulanması önerilir. İki doz arasında geçen süre bir aydan kısa olmamalıdır. Anatomi ve görmeyle ilgili sonuçların hastanın tedaviden fayda görmediğine işaret etmesi halinde EYLEA tedavisi kesilmelidir. Aylık tedavinin maksimum görme keskinliği elde edilene ve/veya hastalık aktivitesine ilişkin belirti kalmayana kadar devam ettirilmesi önerilir. Ardışık üç veya daha fazla aylıkenjeksiyon gerekebilir. Tedavi daha sonra tedavi et ve uzat rejimiyle devam ettirilebilir, görmeyle ilgili ve/veya anatomik sonuçların stabil kalması sağlanarak tedavi aralıkları kademeli şekilde uzatılabilir,ancak bu aralıkların uzunluklarının belirlenmesi için gerekli veriler yetersizdir. Görmeyleilgili ve/veya anatomik sonuçların kötüleşmesi halinde, tedavi aralığı buna uygun şekildekısaltılmalıdır. İzlem ve tedavi programı tedavi eden hekim tarafından hastaya özgü yanıt doğrultusunda belirlenmelidir. 11 / 16 Hastalık aktivitesinin izlemi klinik muayene, fonksiyon testi ya da görüntüleme tekniklerini (örn. optik koherens tomografisi ya da floresan anjiyografi) içerebilir. Diyabetik makula ödemi EYLEA için önerilen tedavi şekli, 50 mikrolitreye (0,05 mL) eşdeğer 2 mg afliberseptin ardışık beş doz olmak üzere ayda bir kez tek enjeksiyonudur ve takiben iki ayda bir tekenjeksiyon olarak devam ettirilmesidir. Hekimin görmeyle ilgili ve/veya anatomik sonuçları değerlendirmesi doğrultusunda tedavi aralığı 2 ay olarak tutulabilir veya bireyselleştirilebilir; örneğin görmeyle ilgili ve/veyaanatomik sonuçların korunması için tedavi aralıklarının genellikle 2 haftalık kademelerleartırıldığı tedavi et ve uzat dozlama rejimi kullanılabilir. Dört aydan daha uzun tedaviaralıkları ile ilgili olarak sınırlı veri bulunmaktadır. Görmeyle ilgili ve/veya anatomiksonuçların kötüleşmesi halinde, tedavi aralığı buna uygun şekilde kısaltılmalıdır. 4 haftadandaha kısa tedavi aralıkları değerlendirilmemiştir (bkz. Bölüm 5.1). İzlem programı tedavi eden hekim tarafından belirlenmelidir. Anatomi ve görmeyle ilgili sonuçların hastanın tedaviden fayda görmediğine işaret etmesi halinde EYLEA tedavisi kesilmelidir. Protokol T çalışma tasarımına göre, EYLEA tedavisi aşağıda belirtilen şekilde uygulanabilir: Aflibersept başlangıçta ve ardından, uygunluk eşiğinin altında bir santral alt alan kalınlığı (SAAK) ile, görme keskinliği (GK) 20/20 ya da daha iyi değilse (Yaklaşık 85 harf değerindeGK skoruna eşdeğer Snellen) ve önceki son iki enjeksiyona cevaben iyileşme ya da kötüleşmeolmamışsa 4 haftada bir enjekte edilmiştir (bkz. Bölüm 5.1). İlk yıl boyunca, takip vizitleriher dört haftada bir (±1 hafta) gerçekleşmiştir. 24. haftadaki vizitten itibaren, görme keskinliği ve SAAK ne olursa olsun, iki ardışık enjeksiyondan sonra iyileşme veya kötüleşme olmamışsa enjeksiyon durdurulmuş, ancakgörme keskinliği harf skoru veya SAAK kötüleşmişse tedavi yeniden başlatılmıştır (bkz.Bölüm 5.1) Miyopik koroidal neovaskülarizasyon EYLEA için önerilen doz 0,05 mL'ye eşdeğer 2 mg aflibersept ile tek bir intravitreal enjeksiyondur. Görmeyle ilgili ve/veya anatomik sonuçlar hastalığın persistan olduğunu düşündürdüğü takdirde ilave dozlar uygulanabilir. Tekrarlama durumunda, hastalık yeni ortaya çıkmış gibitedavi edilmesi önerilir. İzlem programı tedavi eden hekim tarafından belirlenmelidir. İki doz arasında geçen süre bir aydan kısa olmamalıdır. Uygulama şekli:İntravitreal enjeksiyonlar tıbbi standartlar ile geçerli kılavuzlara uygun şekilde ve intravitreal enjeksiyon konusunda deneyimli bir uzman hekim tarafından yapılmalıdır. Genel olarak,yeterli anestezi ve topikal geniş spektrumlu mikrobisit dahil aseptik koşullar (örn. periokülerderi, göz kapağı ve oküler yüzeye povidon iyodür uygulama) sağlanmalıdır. Cerrahi eldezenfenksiyonu, steril eldiven, steril örtü ve steril göz kapağı spekulumu (veya eşdeğeri)önerilmektedir. 12 / 16 Enjeksiyon iğnesi limbusa 3,5-4,0 mm posterior konumdan vitreus boşluğuna batırılmak, yatay meridyenden kaçınılarak kürenin merkezi hedeflenmelidir. Enjeksiyon hacmi 0,05 mLolmalı; sonraki enjeksiyonlar için diğer bir sklera bölgesi kullanılmalıdır. İntravitreal enjeksiyondan hemen sonra hastalar göz içi basınçta artış için kontrol edilmelidir. Uygun takip yöntemi optik sinir başı için perfüzyon kontrolü veya tonometri şeklinde olabilir.Gerektiğinde parasentez için uygun steril ekipman bulundurulmalıdır. İntravitreal enjeksiyondan sonra hastalar endoftalmi düşündüren her türlü semptomu gecikmeden bildirmeleri gerektiği konusunda bilgilendirilmelidir (örn. göz ağrısı, gözdekızarıklık, fotofobi, bulanık görme). Her bir kullanıma hazır enjektör yalnızca tek bir gözün tedavisinde kullanılmalıdır. Tek bir kullanıma hazır enjektörden birden fazla dozun verilmesi kontaminasyon ile bunu takibenenfeksiyon riskini artırabilir. Kullanıma hazır enjektör önerilen 2 mg'lık aflibersept (0,05 mL enjeksiyonluk çözeltiye eşdeğer) dozundan fazlasını içerir. Enjektörden çekilebilen hacim, enjektörden çıkabilenmiktardır ve tümü kullanılmayacaktır. EYLEA kullanıma hazır enjektörden çekilebilecekhacim en az 0,09 mL'dir. Önerilen dozun enjeksiyonundan önce fazla hacim mutlakaatılmalıdır.Kullanıma hazır enjektör içindeki hacmin tamamının enjekte edilmesi doz aşımına neden olabilir. Fazla tıbbi ürünle birlikte hava kabarcığının uzaklaştırılması için piston yavaşçabastırılmak ve piston kubbesinin(kubbenin ucu değil) ile şırınga üzerindeki siyahdozlama çizgisininaynı hizaya gelmesisağlanmalıdır(bkz. Bölüm 4.9 ve 6.6).Enjeksiyondan sonra kullanılmamış olan ürün atılmalıdır. Özel popülasyonlara ilişkin ek bilgiler:Böbrek/Karaciğer yetmezliği:Karaciğer ve/veya böbrek yetmezliği olan hastalarda EYLEA ile ilgili özel bir çalışma yapılmamıştır. Mevcut veriler bu hastalarda EYLEA için dozayarlaması gerektiğine işaret etmemektedir.Pediyatrik popülasyon:EYLEA'nın çocuklarda ve adolesanlarda güvenlilik ve etkililiği belirlenmemiştir. EYLEA'nın yaş tip YBMD, SRVO, RVDO, DMÖ ve miyopik KNVendikasyonları için pediyatrik popülasyonda kullanımı söz konusu değildir.Geriyatrik popülasyon:Doz aşımı ve tedavisiKlinik çalışmalarda aylık aralıklarla verilen 4 mg'a kadar olan dozlar kullanılmış ve 8 mg ile izole doz aşımı olgularına rastlanmıştır. Enjeksiyon hacminin artırılmasıyla gelişen doz aşımı,göz içi basıncın artmasına neden olabilir. Bu nedenle, doz aşımı durumunda göz içi basınçizlenmeli ve tedavi eden hekimin takdirine göre gerekli bulunduğunda, uygun tedaviuygulanmalıdır. 13 / 16 GeçimsizliklerEYLEA diğer tıbbi ürünler ile karıştırılmamalıdır. Saklamaya yönelik özel tedbirler2°C - 8°C arasında (buzdolabında) saklayınız. Dondurmayınız. Açılmamış blister buzdolabının dışında 25°C'nin altında 24 saate kadar saklanabilir. Blister açıldıktan sonra aseptik koşullar altında gerekli işlemlere devam edilmelidir. Işıktan korumak için orijinal ambalajında saklayınız. Ambalajın niteliği ve içeriğiPiston tıpası (elastomerik kauçuk) ve uç kapaklı (elastomerik kauçuk) bir Luer kilit adaptörü ile siyah dozlama çizgisi ile işaretlenmiş kullanıma hazır enjektörde (tip I cam) çözelti. Herbir kullanıma hazır enjektör en az 0,09 mL çekilebilir hacim içerir. Ambalaj boyutu 1kullanıma hazır enjektör. Beşeri tıbbi üründen arta kalan maddelerin imhası ve diğer özel önlemlerKullanılmamış olan ürünler ya da atık materyaller Tıbbi Atıkların Kontrolü Yönetmeliği ve Ambalaj Atıklarının Kontrolü Yönetmeliklerine uygun olarak imha edilmelidir. Kullanıma hazır enjektör sadece tek bir gözün tedavisi için tek kullanımlıktır.Temiz uygulama odasının dışında steril kullanıma hazır enjektör blisterini açmayınız. Kullanıma hazır enjektör, önerilen 2 mg aflibersept dozundan (0,05 mL'ye eşdeğer) fazlasını içerir. Fazla hacim uygulamadan önce dışarı atılmalıdır. Uygulama öncesinde çözelti görsel olarak yabancı partiküler maddeler ve/veya renk bozukluğu veya fiziksel görünüşte herhangi bir değişiklik yönünden incelenmelidir. Herhangibirinin tespit edilmesi durumunda, tıbbi ürün imha edilmelidir. İntravitreal enjeksiyon için bir adet 30 G x 'A inç oftalmik amaçla kalifiye edilmiş enjeksiyon iğnesi kullanılması önerilmektedir. Vitreusta uçuşan noktalar riskini azaltmak için intravitrealenjeksiyonda silikon içermeyen enjeksiyon iğnesi kullanılması önerilmektedir. 14 / 16 Kullanıma hazır enjektörün kullanımı için talimatlar:1. EYLEA'yı uygulamaya hazır olduğunuzda, kutuyu açınız ve steril blister paketini çıkartınız. Blister paketin dışını dikkatle, içindekilerin sterilitesini koruyacak şekilde soyarak açınız. Parçaları birleştirmeye hazır olana kadar enjektörü steril tepsi içinde bırakınız._2. Aseptik teknik kullanarak enjektörü steril blister paketten çıkartınız._3. Enjektör kapağını çıkartmak için bir elinizle enjektörü tutarken diğer elinizi kullanarak başve işaret parmaklarınızla enjektör kapağınısıkıca kavrayınız. Lütfen dikkat: Enjektör kapağını çevirip açınız (kopartmayınız).
4. Ürünün sterilitesini bozmamak için pistonu geri çekmeyiniz.5. Aseptik teknik kullanarak enjeksiyon iğnesini Luer kilitli enjektör ucuna, çevirerek sıkıcatakınız. 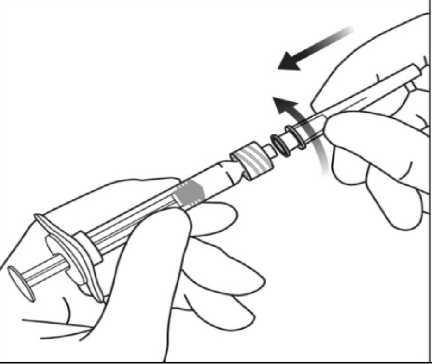 6. İğne yukarı bakacak şekilde enjektörü tutarak enjektörde hava kabarcığı olup olmadığınıkontrol ediniz. Eğer hava kabarcığı varsa,kabarcıklar üst kısma çıkıncaya kadarparmağınızla enjektöre hafifçe vurunuz. 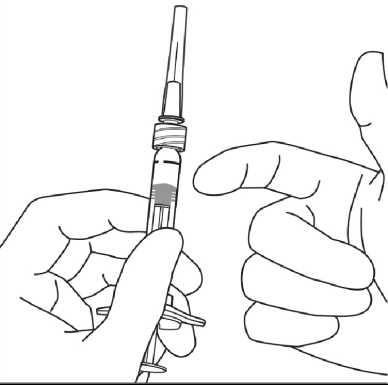
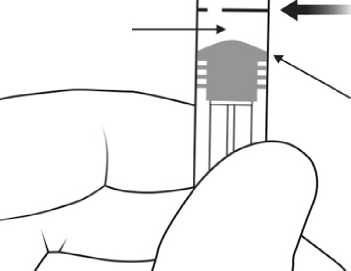
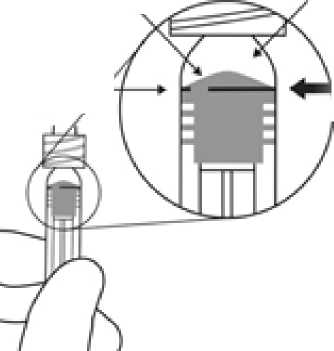
15 / 16 7. Tüm hava kabarcıklarını ve ilacın fazlasını uzaklaştırmak içinpiston kubbesinin tabanı (kubbenin ucu değil) ile şırınga üzerindeki siyah dozlama çizgisiaynı hizaya gelecek şekilde pistona hafifçe bastırınız.Not: Pistonun doğru konumlandırılması çok önemlidir,çünkü yanlışpiston konumlandırması, etikette belirtilen dozdan daha fazlasının veya daha azının verilmesine yol açabilir. 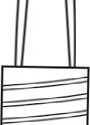 Hava kabarcıkları ve ilacın fazlası uzaklaştırıldıktansonraki kalan çözelti
DozlamaÇizgisi
8. Pistonu dikkatli bir şekilde ve sabit basınçla bastırarak enjekte ediniz. Piston enjektörün dibine ulaştığında daha fazla basınç uygulamayınız. Enjektörde gözlenen çözelti kalıntısıvarsa uygulamayınız._9. Kullanıma hazır enjektör sadece tek kullanımlıktır. Tek bir kullanıma hazır enjektörden çoklu dozların alınması kontaminasyon, sonrasında enfeksiyon riskini artırabilir._
16 / 16 |
İlaç BilgileriEylea 40 Mg/ml İntravitreal Enjeksiyon İçin Çözelti İçeren Kullanıma Hazır EnjektörEtken Maddesi: Aflibersept |
||||||||||
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.