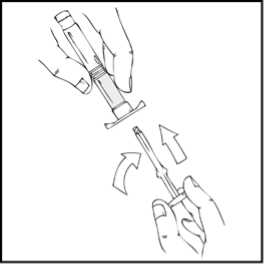
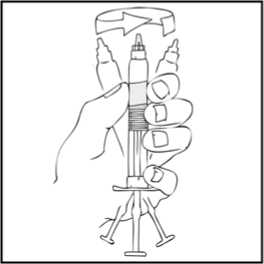
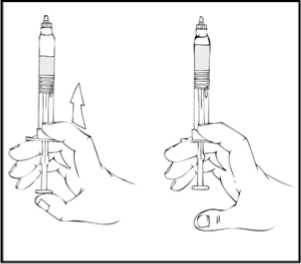
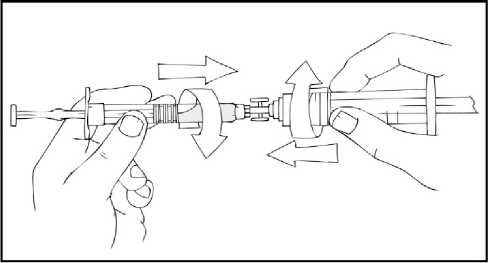
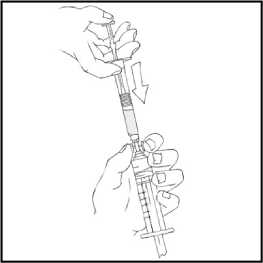
Refacto® Af 2000 Iu Iv Enjeksiyonluk Çözelti İçin Toz ve Çözücü Kullanma TalimatıKULLANMA TALİMATIREFACTO® AF 2000 IU IV enjeksiyonluk çözelti için toz ve çözücü Toplar damar içine uygulanır.Steril Etkin madde:Her kullanıma hazır şırınga 2000 IU moroktokog alfa (rekombinantkoagülasyon faktörü VIII) içermektedir. 4 ml %0,9'luk enjeksiyonluk sodyum klorür çözeltisiile sulandırıldıktan sonra 500 IU/ml moroktokog alfa içerir. Yardımcı madde(ler):Sukroz, kalsiyum klorür dihidrat, L-histidin, polisorbat 80 ve sodyum klorür, enjeksiyonluk su, hidroklorik asit, azot gazı. Çözücü olarak sodyum klorür veenjeksiyonluk su içerir.Bu ilaç ek izlemeye tabidir. Bu üçgen yeni güvenlilik bilgisinin hızlı olarak belirlenmesini sağlayacaktır. Meydana gelen herhangi bir yan etkiyi raporlayarak yardımcı olabilirsiniz. Yan etkilerinnasıl raporlanacağını öğrenmek için 4. bölümün sonuna bakabilirsiniz. Bu ilacı kullanmaya başlamadan önce bu KULLANMA TALİMATINI dikkatlice okuyunuz, çünkü sizin için önemli bilgiler içermektedir. Bu kullanma talimatını saklayınız. Daha sonra tekrar okumaya ihtiyaç duyabilirsiniz. Eğer ilave sorularınız olursa, lütfen doktorunuza veya eczacınıza danışınız. Bu ilaç kişisel olarak sizin için reçete edilmiştir, başkalarına vermeyiniz. Bu ilacın kullanımı sırasında, doktora veya hastaneye gittiğinizde doktorunuza bu ilacıkullandığınızı söyleyiniz. Bu talimatta yazılanlara aynen uyunuz. İlaç hakkında size önerilen dozun dışında yüksekveya düşük doz kullanmayınız.Bu Kullanma Talimatında:1. REFACTO AF nedir ve ne için kullanılır?2. REFACTO AF'yi kullanmadan önce dikkat edilmesi gerekenler3. REFACTO AF nasıl kullanılır?4. Olası yan etkiler nelerdir?5 REFACTO AF'nin saklanmasıBaşlıkları yer almaktadır.1. REFACTO AF nedir ve ne için kullanılır?REFACTO AF kanınızın pıhtılaşmasına yardımcı olan ve kanamayı durduran pıhtılaşma faktörü VIII olarak bilinen bir protein içerir. Hemofili A (doğuştan gelen faktör VIII eksikliği) hastalarında yeterlidüzeyde faktör VIII bulunmamaktadır ya da düzgün şekilde çalışmamaktadır. REFACTO AF kanamaolaylarını düzeltmek ve önlemek için, acil durumlarda, cerrahi müdahale yapılması gereken 1 durumlarda Hemofili A hastalarında, geçici olarak eksik olan pıhtılaşma faktörünün yerine kullanılır. REFACTO AF laboratuvar ortamında rekombinant DNA teknolojisi ile üretilir, kan bağışında bulunankişilerin kanlarından elde edilmez (plazma kaynaklı faktör VIII değildir). REFACTO AF üst bölmede enjeksiyonluk toz, alt bölmede çözücü içeren kullanıma hazır şırınga şeklinde sunulmaktadır. Her paket, 2000 IU moroktokog alfa toz ve sulandırma için 4 ml çözücü (9mg/ml (%0,9) sodyum klorür solüsyonu) ile doldurulmuş 1 adet kullanıma hazır şırınga, 1 adet pistonçubuğu, 1 adet koruyucu havalandırmalı steril kapak, 1 adet steril infüzyon seti, 2 adet alkollütemizleme bezi, 1 adet flaster, 1 adet gazlı bez içerir. 2. REFACTO AF'yi kullanmadan önce dikkat edilmesi gerekenlerREFACTO AF'yi aşağıdaki durumlarda KULLANMAYINIZEğer; Moroktokog alfa'ya ya da REFACTO AF'de yer alan herhangi bir bileşene karşı alerjiniz (aşırıduyarlılığınız) varsa, Hamster proteinlerine karşı alerjik iseniz. Eğer bunlar hakkında emin değilseniz, doktorunuza danışınız. REFACTO AF'yi aşağıdaki durumlarda DİKKATLİ KULLANINIZEğer; Alerjik reaksiyonlarınız varsa. Bazı alerjik reaksiyon belirtileri: Nefes almada güçlük, nefesdarlığı, şişme, kurdeşen, kaşıntı, göğüste daralma hissi, hırıltılı solunum, düşük tansiyon.Anafilaksi, yutma ve/veya nefes alma güçlüğüne, yüz ve/veya ellerde kızarma ve/veya şişmeyeneden olabilen ciddi bir alerjik reaksiyondur. Bu belirtilerden herhangi biri ortaya çıkarsa derhaldamar içine vermeyi (infüzyonu) durdurunuz ve acilen doktorunuza ya da acil servis birimlerinebaşvurunuz. Ciddi alerjik reaksiyon durumlarında alternatif tedavi düşünülmelidir. İnhibitörlerin (antikorlar alerji oluşturan maddeye karşı vücudun ürettiği savunma proteini)oluşumu, tüm faktör VIII ilaçlarıyla tedavi sırasında ortaya çıkabileceği bilinen birkomplikasyondur. Bu inhibitörler, özellikle yüksek seviyelerde, tedavinin düzgün şekildeçalışmasını engeller ve siz veya çocuğunuz bu inhibitörlerin gelişimi açısından dikkatle takipedileceksiniz. Eğer sizin veya çocuğunuzun kanaması REFACTO AF ile kontrol edilmiyorsaderhal doktorunuza bildiriniz. Beklenilenin aksine kanamanız durmazsa, doktorunuza ya da acil servis birimlerine başvurunuz.Takip edilebilirlik Biyolojik ürünlerin takip edilebilirliğinin sağlanması için uygulanan ürünün ticari ismi ve seri numarası mutlaka hasta dosyasına kaydedilmelidir. Bu uyarılar, geçmişteki herhangi bir dönemde dahi olsa sizin için geçerliyse lütfen doktorunuza danışınız. 2 REFACTO AF'nin yiyecek ve içecek ile kullanılmasıGeçerli değildir. Hamilelikİlacı kullanmadan önce doktorunuza veya eczacınıza danışınız.Eğer hamile iseniz, hamile olduğunuzu düşünüyorsanız veya hamile kalmayı planlıyorsanız; ilacı kullanmadan önce doktorunuza danışınız. Kadın hastalarda Hemofili A hastalığı nadir görüldüğünden, REFACTO AF'nin gebe kadınlarda kullanımına ilişkin yeterli veri mevcut değildir. REFACTO AF gebelik döneminde sadece gerekliliği açık olarak belirtilmiş ise kullanılmalıdır. Tedaviniz sırasında hamile olduğunuzu fark ederseniz hemen doktorunuza veya eczacınıza danışınız.Emzirmeİlacı kullanmadan önce doktorunuza veya eczacınıza danışınız.REFACTO AF'nin insan sütüyle atılıp atılmadığı bilinmemektedir. Kadın hastalarda Hemofili A hastalığı nadir görüldüğünden REFACTO AF'nin emzirme döneminde kullanımı ile ilgili yeterli veri mevcut değildir. REFACTO AF laktasyon döneminde sadecegerekliliği açık olarak belirtilmiş ise kullanılmalıdır. Emzirme döneminde iseniz REFACTO AF'yi kullanmadan önce doktorunuza danışınız. Araç ve makine kullanımıREFACTO AF'nin araç veya makine kullanma yeteneği üzerine etkisi bulunmamaktadır. REFACTO AF'nin içeriğinde bulunan bazı yardımcı maddeler hakkında önemli bilgilerSulandırma sonrası her kullanıma hazır şırınga 1,27 mmol (ya da 29 mg) sodyum ihtiva eder. Bu bir yetişkin için önerilen maksimum günlük sodyum alımının %1,5'ine eşdeğerdir. Vücut ağırlığınıza veREFACTO AF dozuna bağlı olarak birden fazla kullanıma hazır şırınga alabilirsiniz. Düşük tuzlu birdiyet yapıyorsanız bu dikkate alınmalıdır. Diğer ilaçlar ile birlikte kullanımıREFACTO AF'nin diğer ilaçlarla etkileştiğine dair bir bilgi yoktur. Eğer reçeteli ya da reçetesiz herhangi bir ilacı şu anda kullanıyorsanız veya son zamanlarda kullandınız ise lütfen doktorunuza veya eczacınıza bunlar hakkında bilgi veriniz.3. REFACTO AF nasıl kullanılır?Uygun kullanım ve doz/uygulama sıklığı için talimatlar:Lütfen bu ilacı her zaman doktorunuzun size söylediği şekilde kullanınız. Emin değilseniz 3 doktorunuza veya eczacınıza danışınız. REFACTO AF ile tedavi, Hemofili A hastalarının tedavisinde deneyimli bir doktor tarafından başlatılmalıdır. Doktorunuz alacağınız REFACTO AF dozunu belirleyecektir. Bu doz ve süre faktörVIII yerine koyma tedavisine bireysel ihtiyacınıza dayanmaktadır. REFACTO AF birkaç dakikalıkenj eksiyon ile bir toplardamar içine verilir. Hastalar veya hasta yakınları uygun şekilde eğitim aldıktansonra REFACTO AF enjeksiyonunu uygulayabilir. Tedavinin dozu ve süresi faktör VIII eksikliğinin derecesine, kanamanın yeri ve süresine ve hastanın klinik durumuna bağlıdır. Uygulanan dozlar hastanın tedaviye verdiği cevaba göre ayarlanmalıdır.Bir inhibitörün (antikorlar alerji oluşturan maddeye karşı vücudun ürettiği savunma proteini)varlığında daha yüksek doz ya da uygun spesifik tedavi gerekebilir. Uygulanacak olan miktar ve uygulama sıklığı daima her hastadaki klinik etkililiğine göre ayarlanmalıdır. Aşağıda durumlara özel istenilen faktör VIII düzeyi (% ya da IU/dl), tedavi süresi (gün) ve dozların sıklığı (saat) yer almaktadır. Kanama durumlarında: Eklem içi kanama, ağızdan ya da kas içine kanama durumlarında; %20-40 (IU/dl) faktör VIII düzeyinde infüzyonu her 12-24 saatte bir tekrarlayınız. Ağrı ile belirlenen kanama atağıdüzelene ya da iyileşme sağlanana kadar en az bir gün kullanınız. Daha yaygın eklem içi kanama, kas içi kanama ya da kanamanın damardan çıkıp doku içerisinde birikmesi durumunda; %30-60 (IU/dl) faktör VIII düzeyinde infüzyonu ağrı ve akutbozukluk düzelene kadar 3-4 gün boyunca veya daha uzun süre her 12-24 saatte birtekrarlayınız. Hayatı tehdit eden kanamalar durumunda ise; %60-100 (IU/dl) faktör VIII düzeyinde infüzyonu tehlike ortadan kalkana kadar her 8-24 saatte bir tekrarlayınız. Cerrahi müdahale olduğu durumlarda: Küçük müdahalelerde (diş çekimi dahil); %30-60 (IU/dl) faktör VIII düzeyinde infüzyonu en az 1 gün olacak şekilde iyileşme sağlanana kadar her 24 saatte bir tekrarlayınız. Büyük müdahalelerde ise %80-100 (IU/dl) faktör VIII düzeyinde infüzyonu (cerrahi öncesinde ve sonrasında); yeterli yara iyileşmesi olana kadar her 8-24 saatte bir tekrar ediniz,daha sonra faktör VIII aktivitesinin %30 ila 60 (IU/dl) olmasını sağlayacak şekilde en az 7gün daha devam ediniz. Kanamaya karşı uzun dönem profilakside (önleyici tedavi) kullanım: 2-3 gün aralıklarla kilogram başına 20-40 IU olacak şekilde kullanılmalıdır. Uygulanacak doz ve tekrarlayan infüzyon sıklığı için yol gösterici olması bakımından tedavi boyunca faktör VIII düzeylerinin takibi önerilir. Özellikle ciddi ameliyatlarda, plazma faktör VIII aktivitesi 4 dikkatli bir şekilde takip edilmelidir. Hastalar faktör VIII'e olan yanıtları bakımından bireysel farklılık gösterebilir. Tedaviniz sırasında doktorunuz, aldığınız REFACTO AF dozunu değiştirmeye karar verebilir. Seyahate çıkmadan önce doktorunuza danışınız. Seyahatiniz sırasında tedaviniz için yeterli olacak miktarda faktör VIII ürününü yanınızda bulundurunuz. Uygulanan faktör VIII'deki birim sayısı, faktör VIII ürünleri için güncel olan WHO normlarına göre Uluslararası Ünite (IU) şeklinde ifade edilir. Plazmadaki faktör VIII aktivitesi yüzde (normal insanplazmasındakine göre) ya da Uluslararası Birim (plazmada faktör VIII için tanımlanmış birUluslararası Standarda göre) olarak gösterilir. Bir IU faktör VIII aktivitesi, 1 ml normal insanplazmasındaki faktör VIII miktarına eşdeğerdir. Gereken faktör VIII dozunun hesaplanması kg olarakvücut ağırlığı başına 1 IU faktör VIII'in plazma faktör VIII aktivitesini 2 IU/dl artırması üzerindenyapılır. Gereken doz aşağıdaki formül üzerinden hesaplanır: Gerekli ünite (IU) = vücut ağırlığı (kg) x istenilen faktör VIII artışı (% ya da IU/dl) x 0,5 (her IU/dl için IU/kg) 0,5 IU/kg (her IU/dl başına) faktör VIII infüzyonlarını takiben genel olarak gözlemlenentoparlanmanın karşılıklılığını temsil eder. REFACTO AF'yi her kullandığınızda ürünün kutu üzerindeki ismini ve seri numarasını kaydetmeniz önerilmektedir. Herhangi bir yan etkinin raporlanması ya da seri numarasını günlüğünüze kaydetmekiçin, kullanıma hazır şırınganın üzerinde bulunan çıkarılabilir etiketlerden birini kullanabilirsiniz. Uygulama yolu ve metodu:REFACTO AF birkaç dakikalık enjeksiyon ile intravenöz yoldan infüzyon (toplar damar içine serum şeklinde) olarak verilir. Değişik yaş grupları:Çocuklarda kullanımı:REFACTO AF yeni doğanlar dahil olmak üzere her yaştan çocukta kullanılabilir. 6 yaşından küçük çocuklarda yetişkinlere göre daha yüksek dozda ilaç uygulanması gerekebilir. Doktorunuzhastalığınıza bağlı olarak ilacınızın dozunu belirleyecek ve size uygulayacaktır. Yaşlılarda kullanımı:REFACTO AF'nin klinik çalışmalarına 65 yaş ve üzerindeki kişiler dahil edilmemiştir. REFACTO AF alan yaşlı hastalarda doz seçimi kişiye özel olmalıdır. Özel kullanım durumları:Böbrek /Karaciğer yetmezliği:Böbrek ya da karaciğer yetmezliği olan hastalarda doz ayarlanması ile ilgili klinik çalışma bulunmamaktadır. Eğer REFACTO AF'nin etkisinin çok güçlü veya zayıf olduğuna dair bir izleniminiz var ise doktorunuz veya eczacınız ile konuşunuz.5 Kullanmanız gerekenden daha fazla REFACTO AF kullandıysanız:REFACTO AF'den kullanmanız gerekenden fazlasını kullanmışsanız bir doktor veya eczacı ile konuşunuz.REFACTO AF'yi kullanmayı unutursanızBir dozu almayı unutursanız, aklınıza gelir gelmez o dozu alınız. Ancak, eğer bir sonraki ilaç alma saatiniz yaklaştıysa atladığınız dozu almayınız. Unutulan dozları dengelemek için çift doz almayınız.REFACTO AF ile tedavi sonlandırıldığındaki oluşabilecek etkilerDoktorunuz tarafından belirtilmedikçe, tedaviyi durdurmayınız. Tedavi, doktor kontrolünde sonlandırılacaktır. Bu ilacın kullanımı hakkında başka sorularınız varsa, doktorunuza veya eczacınıza danışınız. 4. Olası yan etkiler nelerdir?Tüm ilaçlar gibi REFACTO AF'nin içeriğinde bulunan maddelere duyarlı olan kişilerde yan etkiler olabilir. Aşağıdakilerden biri olursa REFACTO AF'yi kullanmayı durdurunuz ve DERHAL doktorunuza bildiriniz veya size en yakın hastanenin acil bölümüne başvurunuz:Alerjik reaksiyonlarEğer şiddetli, ani alerjik reaksiyonlar (anafilaktik) oluşursa, enjeksiyon hemen durdurulmalıdır. Aşağıda belirtilen alerjik reaksiyonların erken belirtilerinden herhangi birini fark ettiğiniz anda,hemen doktorunuzu bilgilendiriniz: Döküntü, kurdeşen, kabarcıklar, genel kaşıntı Dudakların ve dilin şişmesi Nefes almada güçlük, hırıltılı nefes alma, göğüste sıkışma Genel olarak iyi hissetmeme Sersemlik ve bilinç kaybı Nefes almada güçlük ve (neredeyse) bayılma dahil şiddetli belirtiler acil tedavi gerektirir. Ciddi, ani alerjik (anafilaktik) reaksiyonlar yaygın değildir (100 hastanın en fazla 1'ini etkileyebilir) Bunların hepsi çok ciddi yan etkilerdir. Eğer bunlardan biri sizde mevcut ise, sizin REFACTO AF'ye karşı ciddi alerjiniz var demektir. Acil tıbbi müdahaleye veya hastaneye yatırılmanıza gerek olabilir. Inhibitör gelişimiÖnceden faktör VIII içeren ilaçlarla tedavi edilmemiş çocuklar için, inhibitör antikorlar (alerji oluşturan maddeye karşı vücudun ürettiği savunma proteini) (bkz. bölüm 2) çok yaygın oluşabilir (10hastada 1'den fazla); fakat faktör VIII ile daha önce tedavi gören (150 günlük tedaviden daha fazla)hastalarda, risk yaygın değildir (100 hastada 1'den azdır). Bu durum oluşursa, sizin veya çocuğunuzunilaçları düzgün şekilde etki etmeyebilir ve siz veya çocuğunuz sürekli kanama yaşayabilirsiniz. Eğerbu olursa, derhal doktorunuza danışınız. 6 Çok yaygın Yaygın : 10 hastanın en az birinde görülebilir. : 10 hastanın birinden az, fakat 100 hastanın birinden fazla görülebilir. : 100 hastanın birinden az, fakat 1.000 hastanın birinden fazla görülebilir. : 1.000 hastanın birinden az, fakat 10.000 hastanın birinden fazla görülebilir. : 10.000 hastanın birinden az görülebilir. : Eldeki verilerden hareketle tahmin edilemiyor. Yaygın olmayan Seyrek Çok seyrek Bilinmiyor Çok yaygın Daha önce Faktör VIII tedavisi almamış hastalarda inhibitör gelişimi Baş ağrısı Öksürük Eklem ağrısı Ateş Yaygın Kanın damar dışına çıkması (hematom), kanama (hemoraji) Sersemlik İştahta azalma, ishal, kusma, karın ağrısı, bulantı Kurdeşen, döküntü, kaşıntı Kas ağrısı Ürperti hissi, kateter bölgesinde reaksiyon Belirli kan testlerinde (pozitif antikor testi, pozitif anti-faktör VIII antikor testi) faktör VIIIantikorlarında yükselme Yaygın olmayan Daha önce Faktör VIII tedavisi almış hastalarda inhibitör gelişimi (100 hastadan 1'inden az) Ciddi alerjik reaksiyonlar Vücudun bazı kısımlarında (el, ayak vb.) görülen uyuşma, hissizlik, uyuşukluk, yanma hissi,ağrı gibi belirtileri olan bir çeşit sinir kas hastalığı (periferal nöropati), uykululuk hali, tatalmada değişiklik Göğüs ağrısı, hızlı kalp atışı, çarpıntı Düşük tansiyon (hipotansiyon), kan pıhtısı ile ilişkili venlerde (toplardamarlarda) ağrı vekızarıklık, yüzde kızarma Nefes darlığı Aşırı terleme Kuvvetsizlik, ağrı dahil enjeksiyon bölgesi reaksiyonları, enjeksiyon bölgesi iltihaplanması Kalp enzimlerinde hafif yükselme Karaciğer enzimlerinde (aspartat aminotransferaz, alanin aminotransferaz) ve vücutta bulunan(beyin, kalp ve iskelet kaslarında) kreatin fosfokinaz enziminde yükselme, bilirubin düzeyindeartış. 7 Eğer bu kullanma talimatında bahsi geçmeyen herhangi bir yan etki ile karşılaşırsanız doktorunuzu veya eczacınızı bilgilendiriniz.Yan etkilerin raporlanmasıKullanma Talimatında yer alan veya almayan herhangi bir yan etki meydana gelmesi durumunda hekiminiz, eczacınız veya hemşireniz ile konuşunuz. Ayrıca karşılaştığınız yan etkileriwww.titck.gov.tr sitesinde yer alan İlaç Yan Etki Bildirimi ikonuna tıklayarak ya da 0 800 314 0008 numaralı yan etki bildirim hattını arayarak Türkiye Farmakovijilans Merkezi (TÜFAM)'nebildiriniz. Meydana gelen yan etkileri bildirerek kullanmakta olduğunuz ilacın güvenliliği hakkındadaha fazla bilgi edinilmesine katkı sağlamış olacaksınız. 5. REFACTO AF'nin saklanmasıREFACTO AF'yi çocukların göremeyeceği, erişemeyeceği yerlerde ve ambalajında saklayınız.REFACTO AF 2-8°C arası sıcaklıklarda (buzdolabında) saklanmalıdır. Dondurulmamalıdır. Kullanıma hazır şırınga, tek seferlik olmak üzere oda sıcaklığında (25°C'ye kadar) 3 ayı geçmeyecek şekilde saklanabilir. Bu dönemin sonunda ürün buzdolabına geri konulmamalıdır, kullanılmalı ya daatılmalıdır. REFACTO AF'yi buzdolabından çıkardığınız tarihi dış kutunun üzerine not ediniz ve odasıcaklığında saklayınız (25°C'ye kadar). Işıktan korumak için kullanıma hazır şırıngayı dış kutununiçinde saklayınız. Ürünü sulandırdıktan veya gri uç kapağı çıkardıktan sonraki 3 saat içinde kullanınız. Çözelti şeffaf ila hafif opak arasında ve renksiz olmalıdır. Bulanık ya da içinde parçacıklar görülen ürünü kullanmayınız. Son kullanma tarihiyle uyumlu olarak kullanınızAmbalajdaki son kullanma tarihinden sonra REFACTO AF 'yi kullanmayınız.Son kullanma tarihi geçmiş veya kullanılmayan ilaçları çöpe atmayınız! Çevre ve Şehircilik Bakanlığınca belirlenentoplama sistemine veriniz.Çevreyi korumak amacıyla kullanmadığınız REFACTO AF'yi şehir suyuna veya çöpe atmayınız. Bu konuda eczacınıza danışınız.Ruhsat Sahibi:Pfizer PFE İlaçları A Ş. Şişli-İSTANBUL Üretim yeri:Vetter Pharma-Fertigung GmbH & Co. KG, Schuetzenstrasse 87, 99-101 88212 Ravensburg Almanya Bu kullanma talimatıtarihinde onaylanmıştır.8Sulandırarak hazırlama ve uygulamaAşağıda tarif edilen yöntem kullanıma hazır şırınga şeklinde sunulan REFACTO AF'nin hazırlanması ve uygulanması için bir kılavuz niteliğindedir. Hastalar, doktorları tarafından tarif edilen özelhazırlama ve uygulama yöntemlerine uymalıdır. REFACTO AF hazırlandıktan sonra damar içine intravenöz infüzyon yolu ile uygulanır. Kullanıma hazır şırınga 2 bölmeden oluşur; bölmelerden biri REFACTO AF liyofilize tozu ve diğeri çözücüyü [9 mg/mL (%0,9) sodyum klorür çözeltisi] içerir. Bu talimatların anlatımı boyunca, sözkonusu üründen kullanıma hazır şırınga olarak bahsedilecektir. Hazırlama işlemi için yalnızca kutuda sunulan kullanıma hazır şırıngayı kullanın. Uygulama için diğer steril tek kullanımlık şırıngalar kullanılabilir. REFACTO AF diğer infüzyon çözeltileri ile karıştırılarak kullanılmamalıdır. Not:İlave TalimatlarHazırlama1. Aşağıdaki işlemleri gerçekleştirmeden önce daima ellerinizi yıkayınız. 2. Hazırlama işlemi sırasında aseptik (yani temiz ve mikrop içermeyen) teknik kullanılmalıdır. 3. Bu ürünün hazırlanması ve uygulanmasında kullanılan tüm bileşenler, havayla gereksizmaruziyetin minimuma indirgenmesi için steril kapları açıldıktan sonra mümkün olan en kısasürede kullanılmalıdır. Sulandırma1. Kullanıma hazır şırınganın oda sıcaklığına gelmesini bekleyiniz. 2. REFACTO AF kullanıma hazır şırınga kitinin içindekileri çıkartınız ve temiz bir yüzeyekoyarak, ihtiyaç duyacağınız tüm malzemelerin bulunduğundan emin olunuz. 3. Aşağıdaki şekilde gösterildiği gibi piston çubuğunu tutunuz. Piston çubuğunu, REFACTO AFkullanıma hazır şırınganın parmak desteği kısmındaki oyuğun içine doğru, direnç hissedenekadar ittirerek ve saat yönünde çevirerek (yaklaşık 2 kez) sıkıca takınız.
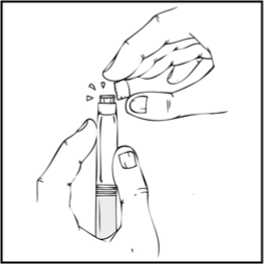
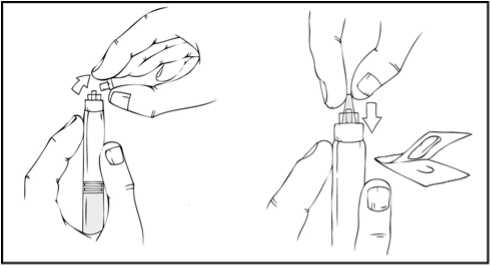
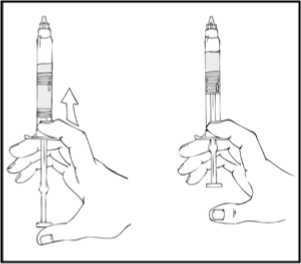
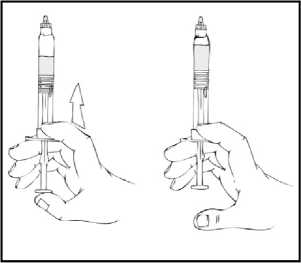
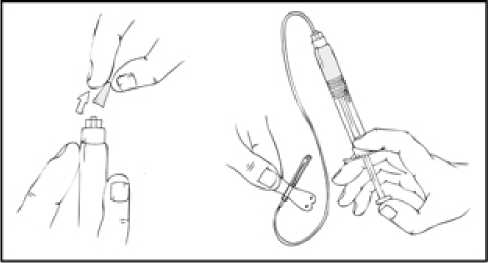
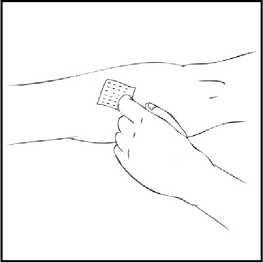
Hazırlama işlemi boyunca, olası sızıntıyı önlemek için REFACTO AF kullanıma hazır şırıngayı dik konumda (beyaz toz, berrak çözeltinin üzerinde olacak şekilde) tutmanızönemlidir. 4. Kullanıma hazır şırıngayı dik tutunuz. Beyaz güvenlik bandını sağdan sola eğerek (veya hafif ileri geri hareket ettirerek) çıkarınız. Kapağın delikli kısmını kırarak gri kauçuk uç kapağını ortaya çıkarınız. 5. Koruyucu mavi havalandırmalı steril kapağı ambalajından çıkartınız. REFACTO AF kullanıma hazır şırıngayı dik tutarak, gri kauçuk uç kapağını çıkartınız ve yerine koruyucu mavi havalandırmalı kapağı takınız. Bu havalandırmalı kapak, basınçoluşmasını önlemek için havanın çıkmasına olanak veren küçük delikler içerir. Şırınganın veyakoruyucu mavi havalandırmalı kapağın açık ucuna dokunmayınız. 6. Kullanıma hazır şırınga içinde iki piston birbirine değene kadar piston çubuğunu nazik veyavaş şekildeilerletiniz ve tüm çözücünün REFACTO AF tozu içeren üst hazneye geçmesinisağlayınız.Not:Şırınganın ucundan sıvının çıkmasını önlemek için, piston çubuğunu ittirirken fazla kuvvet uygulamayınız.10 7. REFACTO AF kullanıma hazır şırıngayı dik tutarak, toz çözünene kadar birkaç kez nazikçedöndürün. Nihai çözeltiyi partikül veya renk değişimi açısından kontrol ediniz. Çözelti, berrak ila hafif opalesan ve renksiz görünüme sahip olmalıdır. Partikül veya renk değişimi gözlenmesidurumunda kullanıma hazır şırıngayı atınız. 8. REFACTO AF kullanıma hazır şırıngayı dik tutarak, havanın tamamını değil fakat büyükkısmını (üst) hazneden çıkartana kadar piston çubuğunu yavaşça ilerletiniz. REFACTO AF, sulandırmayı veya gri uç kapağının kullanıma hazır şırıngadan ayrılmasını izleyen 3 saat içinde infüze edilmelidir. REFACTO AF çözeltisini hemen kullanmayacaksanız, infüzyona hazır olacağınız zamana kadar koruyucu mavi havalandırmalı kapağı kullanıma hazır şırıngaya takarak, şırıngayı dik 11 olarak saklamaksınız. Sulandırılan çözelti, oda sıcaklığında 3 saate kadar saklanabilir. Çözeltiyi 3 saat içinde kullanmadıysanız, atınız. Uygulama (İntravenöz İnfüzyon)Doktorunuz veya diğer sağlık mesleği mensupları, REFACTO AF'nin nasıl kullanılacağını size anlatmalıdır. İnfüzyonu kendi kendinize nasıl uygulayacağınızı öğrendikten sonra, bu kullanmatalimatındaki adımları izleyebilirsiniz. REFACTO AF, tozun çözücüyle (%0,9 sodyum klorür) sulandırılmasından sonra intravenöz (IV) infüzyon yoluyla uygulanır. Sulandırıldıktan sonra uygulanmadan önce REFACTO AF, partikül verenk değişimi açısından kontrol edilmelidir. REFACTO AF, doktorunuz veya diğer sağlık mesleği mensupları tarafından başka türlü önerilmediği sürece, kit içeriğinde bulunan infüzyon seti kullanılarak uygulanmalıdır. 1. Koruyucu mavi havalandırmalı kapağı çıkartınız ve sunulan intravenöz infüzyon setini,REFACTO AF kullanıma hazır şırıngaya sıkı şekilde takınız. 2. Turnike uygulayınız ve deriyi kit içinde sunulan alkollü bezle silerek enjeksiyon bölgesinihazırlayınız. 3. Koruyucu iğne kılıfını çıkartın ve infüzyon setindeki kelebek iğneyi, doktorunuzun veya diğersağlık mesleği mensuplarının söylediği şekilde, toplar damarınızın içine yerleştiriniz. Turnikeyiçıkartınız. Hazırlanmış REFACTO AF ürünü, birkaç dakika süresince intravenöz yolla enjekteedilmelidir. Doktorunuz, infüzyonu daha rahat hale getirmek için size önerilen infüzyon hızını 12 değiştirebilir. İntravenöz infüzyon işleminizi doktorunuzla veya diğer sağlık mesleği mensuplarıyla görüşünüz. Uygun eğitimi almadan kendi kendinize infüzyon uygulamayaçalışmayınız. 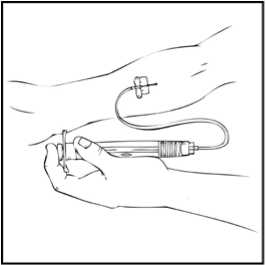 Sulandırılan REFACTO AF, diğer tıbbi ürünlerle aynı tüp veya kap içinde uygulanmamalıdır.4. REFACTO AF infüzyonundan sonra, infüzyon setini çıkartınız ve atınız. İnfüzyon setinde kalantıbbi ürünün miktarı, tedavinizi etkilemeyecektir. Not: Tüm kullanılmayan çözeltiyi, boşalan kullanıma hazır şırıngayı ve kullanılan tıbbi malzemeleri, tıbbi atıkların imhasına uygun bir kapta atınız; bu materyaller, doğru şekildeatılmadığı takdirde başkalarına zarar verebilir. 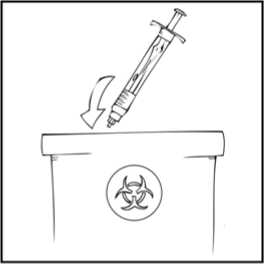 REFACTO AF'yi her kullandığınızda, REFACTO AF kullanıma hazır şırınga etiketinde yer alan lot numarasını kaydetmeniz önerilir. Lot numarasını kaydetmek için REFACTO AFkullanıma hazır şırınga üzerindeki çıkarılabilen etiketi kullanabilirsiniz. 13 İlave Talimatlar:Sulandırılmış Birden Fazla REFACTO AF Kullanıma Hazır Şırınganın 10 cc veya Daha Büyük Luer-lock (kilitli vidalı) Şırıngaya Aktarılması (10 cc veya daha büyük luer-lock (kilitli vidalı)şırıngalar REFACTO AF ambalajı içinde temin edilmemektedir)Aşağıdaki talimatlar, birden fazla REFACTO AF kullanıma hazır şırınga kitlerinin 10 cc veya daha büyük luer-lock (kilitli vidalı) şırıngayla kullanımına yöneliktir. 1. Tüm REFACTO AF kullanıma hazır şırıngaları, yukarıda yer alan sulandırma talimatlarına görehazırlayınız (bkz. Sulandırma ve Uygulama). REFACTO AF kullanıma hazır şırıngayı dik tutarak, havanın tamamını değil fakat büyük kısmını tıbbi ürün haznesinden çıkartana kadar piston çubuğunu yavaşça ilerletiniz. 2. Luer-luer şırınga bağlantısını ambalajından çıkartınız (luer-luer şırınga bağlantıları REFACTO AFambalajı içinde temin edilmemektedir). 3. Steril 10 cc veya daha büyük luer-lock (kilitli vidalı) bir şırıngayı, şırınga bağlantısındakiaçıklıklardan (port) birine ve REFACTO AF kullanıma hazır şırıngayı, diğer uçtaki açık portabağlayınız. 4. REFACTO AF kullanıma hazır şırınga üstte olacak şekilde, içeriği 10 cc veya daha büyük luer-lock (kilitli vidalı) şırıngaya aktarana kadar piston çubuğunu yavaş şekilde ittiriniz. 14 5. Boşalan REFACTO AF kullanıma hazır şırıngayı çıkartınız ve yukarıda sunulan 3. ve 4. adımdakiişlemleri diğer sulandırılmış şırıngalar için tekrarlayınız. 6. Luer-luer şırınga bağlantısını 10 cc veya daha büyük luer-lock (kilitli vidalı) şırıngadan çıkartın vekullanıma hazır şırınganın uygulanmasına ilişkin yukarıda açıklanan talimatlara uygun olarakinfüzyon setini bağlayınız [bkz. Uygulama (İntravenöz İnfüzyon)]. Not:Tüm kullanılmayan çözeltiyi, boşalan kullanıma hazır şırıngayı ve kullanılan tıbbi malzemeleri, tıbbi atıkların imhasına uygun bir kapta atınız; bu materyaller, doğru şekilde atılmadığı takdirdebaşkalarına zarar verebilir.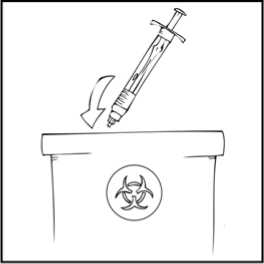
15 |
İlaç BilgileriRefacto® Af 2000 Iu Iv Enjeksiyonluk Çözelti İçin Toz ve ÇözücüEtken Maddesi: Moroktokog Alfa (rekombinant Koagülasyon Faktörü Viii) Kullanma talimatı ve kısa ürün bilgileri
Google Reklamları
İlgili İlaçlar |
Ana Sayfa | Hakkımızda | İlaçlar | İlaç Ara | İlaç Firmaları | Gizlilik | Bize Ulaşın
Telif Hakkı 2008-2026 © İlaç Prospektüsü. Tüm Hakları Saklıdır.Uyarı: Sitemizde yayınladığımız ilaç bilgileri ile doktora danışmadan kesinlikle ilaç kullanmayınız!
Aksi halde doğabilecek sağlık sorunlarından ilacprospektusu.com sorumlu tutulamaz.