KULLANMA TALİMATIULVEST®250 mg/5 mL Enjeksiyonluk Çözelti İçeren Kullanıma Hazır Enjektör Kas içine uygulanır.
Sterildir.
Etkin madde:Her bir kullanıma hazır enjektör 5 mL çözeltide etkin madde olarak250 mg fulvestrant içerir.
Yardımcı maddeler:Etanol %96, benzil alkol, benzil benzoat, rafine hintyağı
Bu ilacı kullanmaya başlamadan önce bu KULLANMA TALİMATINI dikkatlice okuyunuz, çünkü sizin için önemli bilgiler içermektedir.
Bu kullanma talimatım saklayınız. Daha sonra tekrar okumaya ihtiyaç duyabilirsiniz.
Eğer ilave sorularınız olursa, lütfen doktorunuza veya eczacınıza danışınız.
Bu ilaç kişisel olarak sizin için reçete edilmiştir, başkalarına vermeyiniz.
Bu ilacın kullanımı sırasında, doktora veya hastaneye gittiğinizde doktorunuza bu ilacıkullandığınızı söyleyiniz.
Bu talimatta yazılanlara aynen uyunuz. İlaç hakkında size önerilen dozun dışındayüksekveya düşükdoz kullanmayınız.Bu Kullanma Talimatında:
1. UL VEST®nedir ve ne için kullandır?
2. UL VEST®'i kullanmadan önce dikkat edilmesi gerekenler
3. UL VEST®nasıl kullandır?
4. Olası yan etkiler nelerdir?
5. UL VEST9 'in saklanmasıBaşkklan yer almaktadır.1. ULVEST® nedir ve ne için kullandır?
ULVEST®, emniyet halkalı kapak düzeneğine sahip kullanıma hazır enjektör içerenambalajlarda kullanıma sunulmaktadır. Enjektörün gövdesine bağlamak için güvenlibir iğne (SafetyGlide) de verilmektedir.
ULVEST® her kullanıma hazır enjektörde 5 mL çözelti içerisinde etkin madde olarak250mg fulvestrant içerir. ULVEST®, berrak, renksiz ila san renkte, viskoz çözeltidir.
ULVEST® östrojen reseptör blokörleri (östrojenin bağlanarak aktifleştirdiği bir takımproteinleri inhibe eder) olarak adlandmlan bir ilaç grubuna dahildir. Kadın cinsiyethormonlarından biri olan östrojenler bazı durumlarda meme kanserinin büyümesinderol oynayabilir.
ULVEST®,
tek başma, hormon reseptörü pozitif, insan epidermal büyüme faktörü reseptörü-2negatif meme kanseri denen bir meme kanseri tipinin lokal olarak ilerlemiş veyavücudun başka bölgelerine yayılım (nkbtdstİ8ik)5goStfeli^ tflitaak itefflMMtanı^ötoldÜğöi,
Belge l>hjBth©ıkdnfidri: JçfiV(^i\oMobıt»döKtW'Mâkvi'(Köölöjıffllödavi) ahnitelş?ifid0öpbda?si:https://www.turkiye.gov.tr/saglik-titck-ebys girmiş olan kadınların tedavisinde, girmiş olan kadınların tedavisinde,
tek başına, daha önce erken evre veya vücudun başka yerlerine yayılım göstermiş olan
1
meme kanseri (adjuvan veya metastatik hastalık) için uygulanan antiöstrojen tedavisi sırasında ya da sonrasında meme kanseri tekrar nüks eden (ortaya çıkan) menopozagirmiş olan kadınların tedavisinde,
bir CDK 4/6 inhibitörü (siklin bağımlı kinaz 4/6 baskılayıcısı) ile kombinasyonhalinde, hormon reseptörü pozitif, insan epidermal büyüme faktörü reseptörü-2 negatifmeme kanseri denen bir meme kanseri tipinin lokal olarak ilerlemiş veya vücudunbaşka bölgelerine yayılım göstermiş olan formunun görüldüğü, meme kanseri içindaha önce endokrin tedavi almamış, menopoza girmiş olan kadınların tedavisinde,
bir CDK 4/6 inhibitörü ile kombinasyon halinde, hormon reseptörü pozitif, insanepidermal büyüme faktörü reseptörü-2 negatif meme kanseri denen bir meme kanseritipinin lokal olarak ilerlemiş veya vücudun başka bölgelerine yayılım göstermiş olanformunun görüldüğü, meme kanseri için daha önce endokrin tedavi almış, menopozagirmiş olan kadınların tedavisinde kullanılır.
ULVEST® CDK 4/6 inhibitörü ile kombinasyon halinde verildiğinde, ilgili CDK 4/6 inhibitörü kullanma talimatını da okumanız önemlidir. CDK 4/6 inhibitörü hakkında herhangibir sorunuz varsa lütfen doktorunuza danışın.2. ULVEST®'i kullanmadan önce dikkat edilmesi gerekenlerULVEST®'i aşağıdaki durumlarda KULLANMAYINIZ
Eğer:
Fulvestrant veya ULVEST®'in bileşiminde bulunan yardımcı maddelerdenherhangi birine karşı (yardımcı maddeler listesine bakınız) alerjiniz varsa,
Hamileyseniz veya emzirme dönemindeyseniz,
Ciddi karaciğer problemleriniz varsa.ULVEST®'i aşağıdaki durumlarda DİKKATLİ KULLANINIZ
Eğer:
Böbrek veya karaciğer problemleriniz varsa,
Kandaki trombosit (kan pulcuğu; kan pıhtılaşmasını sağlayan kan hücresi) sayınızdüşükse ya da kanama bozukluğunuz varsa,
Kan pıhtılaşması problemleriniz varsa,
Kemik erimeniz (osteoporoz, kemik yoğunluğu kaybı) varsa,
Alkolizm problemleriniz varsa.
Bu uyanlar geçmişteki herhangi bir dönemde dahi olsa sizin için geçerliyse lütfen doktorunuza danışınız.ULVEST®'in yiyecek ve içecek ile kullanılması
ULVEST®'in yiyecek ve içeceklerle etkileşimi yoktur.
Hamilelik
İlacı kullanmadan önce doktorunuza
danışınız.
|
 |
Iresı'https://www. turkiye.gov.tr/saglik-titck-ebys |
ile tedavi edilirken ve aldığınız son dozdan sonraki 2 yıl süresince etkili bir doğum kontrol yöntemi kullanmalısınız. |
2
Tedaviniz sırasında hamile olduğunuzu fark ederseniz hemen doktorunuza veya eczacınıza danışınız.Emzirme
İlacı kullanmadan önce doktorunuza veya eczacınıza danışınız.
ULVEST® ile tedavi edilirken bebek emzirmemelisiniz.Araç ve makine kullanımı
ULVEST®'in araç ve makine kullanma yeteneğinizi etkilemesi beklenmemektedir.
Ancak tedaviden sonra kendinizi yorgun hissediyorsanız araç veya makine kullanmayınız.ULVEST®'in içeriğinde bulunan bazı yardımcı maddeler hakkında önemli bilgiler
ULVEST®'te hacmin %10'u kadar etanol (alkol) vardırT (örneğin, her enjektörde 500 mg'a kadar, her enjeksiyonda 10 mL biraya eşdeğer, her enjeksiyonda 4 mL şarabaeşdeğer gibi). Alkol bağımlılığı olanlar için zararlı olabilir. Karaciğer hastalığı ya daepilepsi gibi yüksek risk grubundaki hastalar için dikkate alınmalıdır.
ULVEST®, her enjeksiyonda 1 ml'sinde 100 mg'a eşdeğer 500 mg benzil alkol (90 mg/kg/gün'den daha az) içermektedir. Benzil alkol, aleıjik reaksiyonlara sebep olabilir.Diğer ilaçlar ile birlikte kullanımı
Özellikle pıhtılaşmayı önleyen bir ilaç (antikoagülan) kullanıyorsanız mutlaka doktorunuza bilgi veriniz.
Eğer reçeteli ya da reçetesiz herhangi bir ilacı şu anda kullanıyorsanız veya son zamanlarda kullandıysanız lütfen doktorunuza veya eczacınıza bunlar hakkında bilgi veriniz.3. ULVEST® nasd kullandır?Uygun kullanım ve doz/uygulama sıklığı için talimatlar:
ULVEST®'in, yaşlılar dahil erişkin yaştaki kadınlar için önerilen dozu ayda bir kez iki 5 mlTik enjeksiyon olarak, uygulanan toplam 500 mg ve bir defaya mahsus olarak ilk dozdaniki hafta sonra verilen ilave bir 500 mg dozdur.Uygulama yolu ve metodu:
ULVEST®, bir doktor veya hemşire tarafından kalçaya, kas içine yavaşça enjeksiyon yapılarak uygulanır.
ULVEST®'in nasıl uygulanacağı konusunda, bu kılavuzun sonunda bulunan ve sağlık personeli için hazırlanan bölüme bakınız.Değişik yaş gruplan:Çocuklarda ve ergenlerde kullanımı:
Güvenlilik ve etkililiğin bu yaş grubunda değçKİBOfhlilnaemİB Qİ»a6lınfidf«uylieeUL¥E&T®şİO . 18 Be3P Rİtşd^ıSQWMaildfl\VeK^WgGSftfir4Ç/kWİİawta<tŞMWOlsto0jnpktpdİr. Belge Takip Adresi:https://www.turkiye.gov.tr/saglik-titck-ebysYaşlılarda kullanımı:
3
ULVEST®'in, yaşlılar için önerilen dozu, ayda bir kez iki 5 ml'lik enjeksiyon olarak, uygulanan toplam 500 mg ve bir defaya mahsus olarak ilk dozdan iki hafta sonra verilen ilavebir 500 mg dozdur.Özel kullanım durumları:Böbrek yetmezliği:
Hafif ila orta derecede böbrek yetmezliğiniz varsa doz ayarlaması önerilmemektedir.
İleri derecede böbrek yetmezliği olan hastalarda ULVEST®'in güvenlilik ve etkililiği değerlendirilmediğinden bu hastalarda dikkatli olunması önerilmektedir.Karaciğer yetmezliği:
Hafif ila orta derecede karaciğer yetmezliğiniz varsa doz ayarlaması önerilmemektedir.
İleri derecede karaciğer yetmezliği olan hastalarla ilgili veri mevcut değildir. Bu nedenle ULVEST® ileri derecede karaciğer yetmezliği olan hastalarda kullanılmamalıdır.
Eğer UL VEST® 'in etkisinin çok güçlü veya zayıf olduğuna dair bir izleniminiz var ise
doktorunuz veya eczacınız ile konuşunuz.Kullanmanız gerekenden daha fazla ULVEST® kullandıysanız
ULVEST®'ten kullanmanız gerekenden fazlasını kullanıldığına dair bir hissiniz varsa bir doktor veya eczacı ile konuşunuz.ULVEST®'i kullanmayı unutursanız
Unutulan dozları dengelemek için çift doz uygulamayınız.ULVEST® ile tedavi sonlandınldığmda oluşabilecek etkiler
Bilgi bulunmamaktadır.4. Olası yan etkiler nelerdir?
Tüm ilaçlar gibi, ULVEST®'in içeriğinde bulunan maddelere duyarlı olan kişilerde yan etkiler olabilir.Aşağıdakilerden biri olursa ULVEST®'i kullanmayı durdunuz ve DERHAL doktorunuza bildiriniz veya size en yakın hastanenin acil bölümüne başvurunuz:
Alerjik reaksiyonlar (aşın duyarlılık): anafilaksinin belirtileri olabilecek yüz, dudak, dilve/veya boğazın şişmesi
Tromboembolizm (kan pıhtılaşma riskinde artış)* (Bacaklarda olursa; ağn, şişme, ısıartışı ve kızarıklık, akciğerlerde olursa; ani göğüs ağnsı, nefes darlığı, öksürükle kangelmesi ve bilinç kaybı ile kendim gösterebilir)
Karaciğerde inflamasyon (karaciğer iltihabı)
Karaciğer yetmezliği
Bunların hepsi çok ciddi yan etkilerdir. Bu belge Be6ğeribÜnlht^^4)irilsMl:vıi(©^i:'ut<i^e;ıSfi!İh\t®VE,$T^tfe''kh'r^brâlli'aler|'inizdâtldenlıektİr.vdresi:lıUps: www.nirkiye.gov.tr saglik-titck-ebysAcil tıbbi müdahaleye veya hastaneye yatınlmamza gerek olabilir.
4
Diğer yan etkiler aşağıdaki kategorilerde gösterildiği şekilde sıralanmıştır:
Çok yaygm: 10 hastanın en az 1 'inde görülebilir.
Yaygın: 10 hastanın birinden az, fakat 100 hastanın birinden fazla kişide görülebilir.
Yaygm olmayan: 100 hastanın birinden az, fakat 1.000 hastanın birinden fazla kişide görülebilir.
Seyrek: 1.000 hastanın birinden az, fakat 10.000 hastanın birinden fazla kişide görülebilir.
Çok seyrek: 10.000 hastanın birinden az kişide görülebilir.
Bilinmiyor: Eldeki verilerden hareketle tahmin edilemiyor.
Çok yaygın yan etkiler
Enjeksiyon bölgesi ağrısı ve iltihap dahil enjeksiyon bölgesi reaksiyonları
Karaciğer enzimlerinde artış (kan testlerinde)1
Bulantı (hasta hissetme hali)
Halsizlik, kuvvetsizlik1
Eklem ağrısı ve kas, iskelet ağrısı
Sıcak basmaları
Cilt döküntüsü
Yüzde, dudaklarda, dilde ve/veya boğazda şişkinliği içeren aleıjik reaksiyonlar (aşınduyarlılık reaksiyonlan)
Yaygm yan etkiler
Baş ağnsı
Kusma, ishal, iştahsızlık1
İdrar yolu enfeksiyonu
Sırt ağnsı1
Bilirubin seviyesinde artış (karaciğerin ürettiği safra pigmenti)
Tromboembolizm (artmış kan pıhtılaşması riski)1
Trombosit düzeylerinde düşüş (trombositopeni)
Vajinal kanama
Tek tarafta bacağa uzanan bel ağnsı (siyatik)
Bacakta, özellikle vücudun yalmzca tek tarafında, ani güçsüzlük, hissizlik,karıncalanma veya hareket kaybı, yürüme veya dengeyle ilgili aniden ortaya çıkanproblemler (periferik nöropati)
Dudak, dil ve/veya gırtlakta şişlik
Yaygm olmayan yan etkiler
Vajinal kandidiyazis (vajinada oluşan bir tür mantar hastalığı), koyu beyazımtırak akıntı
Enj eksiyon bölgesinde şişlik ve kanama
Kas ağrısı
Vertigo (denge bozukluğundan kaynaklanan baş dönmesi)
Lökopeni (akyuvar sayısında azalma)
Gamma-GT'de (kan testinde görülen bir karaciğer enzimi) artış
Karaciğer iltihabı (hepatit)
Karaciğer yetmezliği
Uyuşukluk, karıncalanma ve ağn Bu belge güVenli elektronik imza ile imzalanmıştır.
Yan etkilerin raporlanması
Kullanma Talimatında yer alan veya almayan herhangi bir yan etki meydana gelmesi durumunda hekiminiz, eczacımz veya hemşireniz ile konuşunuz. Ayrıca yan etkileriwww.titck.gov.tr sitesinde yer alan İlaç Yan Etki Bildirimi ikonuna tıklayarak ya da O 800314 00 08 numaralı yan etki bildirim hattını arayarak Türkiye Farmakovijilans Merkezi(TÜFAM)'ne bildiriniz. Meydana gelen yan etkileri bildirerek kullanmakta olduğunuz ilacmgüvenliliği hakkında daha fazla bilgi edinilmesine katkı sağlamış olacaksınız. sitesinde yer alan İlaç Yan Etki Bildirimi ikonuna tıklayarak ya da O 800314 00 08 numaralı yan etki bildirim hattını arayarak Türkiye Farmakovijilans Merkezi(TÜFAM)'ne bildiriniz. Meydana gelen yan etkileri bildirerek kullanmakta olduğunuz ilacmgüvenliliği hakkında daha fazla bilgi edinilmesine katkı sağlamış olacaksınız.
Eğer bu kullanma talimatında bahsi geçmeyen herhangi bir yan etki ile karşılaşırsanız doktorunuzu veya eczacınızı bilgilendiriniz.5. ULVEST®'in saklanması
ULVESl®'i çocukların göremeyeceği, erişemeyeceği yerlerde ve ambalajında saklayınız.
2°C - 8°C arasında (buzdolabında) saklayınız.
2-8°C dışındaki sıcaklık değişimleri smılandmlmalıdır. 25C'yi aşan sıcaklıklarda stoklama önlenmelidir ve 25°C'nin altındaki ürün (ama 2-8°C'nin üzerinde) için ortalama saklamasıcaklığı 28 günlük periyodu aşmamalıdır. Sıcaklık değişimlerinin ardından ürün hızlı birşekilde önerilen saklama koşullarına getirilmelidir (2-8°C'de taşınmalıdır ve saklanmalıdır).Sıcaklık değişimlerinin ürünün kalitesi üzerinde kümülatif etkisi vardır ve 28 günlük süre 2yıllık raf ömrü boyunca aşılmamalıdır. 2°C'nin altındaki sıcaklığa maruz kalınması, -20°C'ninaltında muhafaza edilmemesi koşuluyla ürüne zarar vermez. Işıktan korumak için kullanımahazır enjektörü orijinal ambalajında saklayınız.Son kullanma tarihiyle uyumlu olarak kullanınız.
Ambalajdaki son kullanma tarihinden sonra ULVESİ®'i kullanmayınız.Son kullanma tarihi belirtilen ayın son günüdür.
Eğer üründe ve/veya ambalajmda bozukluklar fark ederseniz ULVEST*'i kullanmayınız.
Çevreyi korumak amacıyla, kullanılmayan şırıngaları şehir suyuna veya çöpe atmayınız. Bu konuda eczacınıza danışınız.
Son kullanma tarihi geçmiş veya kullanılmayan ilaçlan çöpe atmayınız! Çevre ve Şehircilik Bakanlığınca belirlenen toplama sistemine veriniz.
Ruhsat Sahibi:
Teva İlaçlan San. ve Tic. AŞ. Ümraniye/lstanbul
Üretim Yeri:
Pliva Croatia Ltd. Zagreb/Hırvatistan
5
gjsumtlanrnı
_______ ja talimatı 24
'oğrıılama Kodu: İZ
56ZW5ı
6
XAŞAĞIDAKİ BİLGİLER ULVEST®'i UYGULAYACAK SAĞLIK PERSONELİ İÇİNDİR
ULVEST® 500 mg, (2 x 250 mg/5 mİ Enjeksiyonluk çözelti) 2 adet kullanıma hazır enjektör ile uygulanır.
Uyan - Kullanım öncesinde güvenli iğneyi (BD SafetyGlide Koruyucu Hipodermik İğne) otoklavlamaym. Kullamm ve imha sırasında eller daima iğnenin arkasında durmalıdır.
Her iki enjektör için:
Cam enjektör gövdesini, tepsiden alm ve hasar |
Şekil l |
|
görüp görmediğini kontrol edin. |
|
n |
Güvenli iğnenin (Safety-Glıde) dış ambalajım açm. |
|
'V |
Parenteral çözeltiler uygulama öncesi partiküler |
|
|
madde ve renk değişimi açısından görsel olarak |
|
r
: |
incelenmelidir. |
* |
cBa |
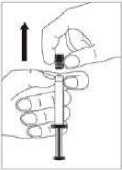
Şırıngayı oluklu kısmından (C) dik olarak tutun. Diğer elinizle başlığı (A) tutun ve dikkatlicebaşlık aynlıp çıkanlabilene kadar ileri geri eğin,çevirmeyin (Şekil 1 'e bakınız).
Şekil 2 |
 |
Şekil 3 + |
 |
Başlığı (A) düz olarak yukan yönde çıkann. Steriliteyi korumak için şınnga ucuna (B)dokunmayın (Şekil 2'ye bakınız).
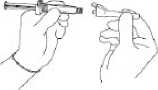
Güvenli iğneyi Luer-Lok'a bağlayın ve tam olarak oturana kadar çevirin (Şekil 3'e balanız).
Dikey düzlemi değiştirmeden önce iğnenin Luer bağlantı yerine kilitlenmiş olduğunu kontrol edin.
dümdüz çekerek çıkann.
idu: lZW56ZW56ZmxXZW56M0FySHY3S3k0ZlAx
İğnenin kılıfım, ucuna zarar vernıemek için dümdüz ,
Belge Do
Dolu enjektörü uygulama noktasına getirin.
İğnenin üzerindeki koruyucu kılıfı çıkann.
7
Enjektörün içerisindeki havayı alın.
Şekil 4
Şekil 5 |
 |
Kalçaya (gluteal bölge), intramusküler
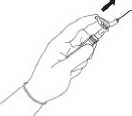
enjeksiyon olarak yavaşça uygulayın (1-2 dakika/enjeksiyon).Kullanıcıya kolaylık
sağlanması açısından iğnenin ucu, kesik ağzı yukarıya bakacak şekilde, enjektörün üzerindekikola sabitlenmiştir (Şekil 4'ebakınız).
İğneyi hastadan çeker çekmez, enjektörünüzerindeki kolu tamamen ileriye doğru, iğneninucu örtülünceye kadar iterek iğne korumadüzeneğini çalıştırın (Şekil 5'e balanız).
NOT: Görsel olarak, plastik kolun tamamenilerlemiş olduğunu ve iğne ucunun kapandığımdoğrulayınız. Bunu gerçekleştiremezseniz,enjektörü hemen, içerisine keskin cisimlerinkonulduğu bir kutuya atın.
Doldurulmuş şırıngalaryalnızca tek kullanımiçindir. Kullanılmayan tıbbi ürünler veya atık maddeler, yerelyönetmeliklere uygun olarak atılmalıdır.
8
9
1
Bu yan etkilerde, altta yatan diğer hastalıklar nedeniyle, ULVEST®'in kesin rolü değerlendirilememektedir.
|
|





